
INTRODUCTION
Le SIBO, ou prolifération bactérienne de l’intestin grêle, est un trouble connu, mais les recherches sur son fonctionnement et sur l’intestin dans son ensemble deviennent de plus en plus précises. Ces avancées permettent de mieux comprendre sa complexité, ses causes profondes et l’impact d’un déséquilibre sur tout le système digestif.
Contrairement au côlon, lieu naturel de fermentation, l’intestin grêle est un organe d’assimilation. Quand il devient un site de fermentation, c’est le début des ballonnements, douleurs et troubles digestifs.
Pour comprendre le SIBO, il faut le replacer dans l’ensemble du parcours digestif : bouche, estomac, foie, pancréas, intestin… chaque organe fonctionne en cascade, et un dysfonctionnement peut déséquilibrer tout le système.
Parcourons ensemble les dernières avancées scientifiques et les solutions intégratives adaptées aux différentes formes de SIBO : H₂, CH₄ et H₂S. Un regard global est essentiel pour appréhender ce trouble, rétablir l’équilibre et soutenir la digestion de manière efficace !
Physiopathologie du SIBO
En situation normale, la concentration bactérienne de l’intestin grêle reste très faible, inférieure à 10³ unités par millilitre, limitant la fermentation et préservant l’intégrité de la muqueuse. Dans le SIBO, cette régulation est rompue : la prolifération excessive de bactéries entraîne une fermentation prématurée des sucres et la production de gaz (hydrogène, méthane, sulfure d’hydrogène).
Ces métabolites gazeux exercent une pression mécanique et biochimique sur une muqueuse peu adaptée, favorisant l’hyperperméabilité intestinale. L’exposition accrue de la barrière intestinale aux endotoxines et fragments bactériens déclenche alors une inflammation de bas grade et une activation immunitaire chronique, contribuant à la symptomatologie digestive (ballonnements, douleurs, diarrhée ou constipation) et systémique du SIBO.
Sur le long terme cela peut engendrer une malabsorption importante des nutriments, notamment des glucides, des graisses, des protéines et du fer, ce qui peut conduire à des carences nutritionnelles et à un état de dénutrition ou le développement d’autres pathologies comme l’obésité, la maladie cœliaque, le syndrome du côlon irritable, des lésions hépatiques, etc.
Distinction fonctionnelle : intestin grêle vs côlon
Souvent regroupés à tort sous une même approche digestive, le côlon et l’intestin grêle jouent pourtant des rôles très différents. L’intestin grêle est avant tout un lieu d’assimilation : ses parois, plus perméables et richement vascularisées, permettent l’absorption des nutriments essentiels. Le microbiote de l’intestin grêle (MIG), plus restreint mais hautement spécialisé— intervient dans la digestion, la modulation immunitaire et le métabolisme des nutriments.
À l’inverse, le côlon est un territoire de fermentation. Son environnement plus dense en mucus et en bactéries favorise la dégradation des fibres non digérées et la production d’acides gras à chaîne courte bénéfiques.
Le microbiote colique et le microbiote de l’intestin grêle (MIG) répondent à des équilibres très différents : chacun mérite une approche spécifique, tant dans la compréhension de ses fonctions que dans les stratégies de rééquilibrage.
Altérations des réseaux microbiens
Au-delà de la simple prolifération bactérienne, le SIBO s’accompagne d’une profonde désorganisation du réseau microbien du duodénum (1). Les interactions symbiotiques qui assurent la cohésion, la communication et la régulation fonctionnelle des communautés microbiennes sont altérées. Cette perte de connectivité compromet la production de métabolites bénéfiques, la modulation de la réponse immunitaire locale et la digestion optimale des nutriments.
La désorganisation des réseaux favorise l’émergence de souches opportunistes au détriment de symbiotes clés, appauvrissant la diversité fonctionnelle et accentuant l’instabilité de l’écosystème intestinal (2). Plus que la perte de diversité elle-même, c’est cette rupture des communications microbiennes qui explique la complexité clinique du SIBO et justifie une approche thérapeutique globale visant à restaurer l’équilibre écologique et la résilience microbienne.
Envisager l’ensemble du parcours digestif
Le SIBO ne peut se comprendre isolément : il est le reflet d’un déséquilibre global du système digestif, et chaque étape du parcours, de la bouche au côlon, joue un rôle clé dans sa prévention ou son aggravation.
L’estomac et son acidité limitent l’entrée des microbes indésirables. La bile et les enzymes pancréatiques participent à leur élimination tout en assurant la digestion. Le complexe migrant moteur nettoie l’intestin entre les repas, tandis que la valve iléo-caecale empêche les bactéries du côlon de remonter. Enfin, le système immunitaire intestinal veille à l’équilibre global du microbiote.
Quand l’un de ces maillons faiblit, c’est tout le parcours qui se dérègle, transformant l’intestin grêle qui est un lieu d’assimilation, en terrain de fermentation.
Comprendre le SIBO, c’est donc envisager la digestion comme un tout cohérent, où chaque organe a sa part d’équilibre.
Distinguer pour mieux solutionner
- Le SIBO (Small Intestinal Bacterial Overgrowth) correspond à une surcroissance de bactéries pathobiontes dans l’intestin grêle (jéjunum ou iléon), dépassant 10⁵ CFU/mL. Il s’accompagne souvent d’un appauvrissement du microbiote et d’un déséquilibre des réseaux microbiens.
- Le SIFO (Small Intestinal Fungal Overgrowth) désigne une prolifération fongique, le plus souvent de Candida spp., au niveau de l’intestin grêle.
- Le LIBO (Large Intestinal Bacterial Overgrowth) concerne, lui, le gros intestin, avec une flore colique altérée et une production de méthane fréquemment accrue.
- L’IBS (syndrome de l’intestin irritable) est un trouble fonctionnel marqué par des douleurs abdominales et des perturbations du transit, généralement sans surcroissance microbienne clairement identifiée.

ZOOM SUR LE SIBO
Les Trois Visages du SIBO
Lorsqu’on parle de SIBO, on fait généralement référence au SIBO hydrogène (H₂). Cependant, les avancées scientifiques ont permis de mieux caractériser les déséquilibres du microbiote intestinal, et de distinguer trois configurations principales selon le type de gaz produit : le SIBO hydrogène (H₂), le SIBO méthanogène (CH₄), et le SIBO hydrogène sulfureux (H₂S).
Ces formes dépendent de la présence et de la prolifération de « taxons perturbateurs microbiens », capables de produire différents gaz au cours de la fermentation des substrats alimentaires (3).
Ainsi, certaines bactéries (comme E. coli ou Klebsiella) sont majoritairement productrices d’hydrogène, alors que des archées méthanogènes (comme Methanobrevibacter smithii) transforment cet hydrogène en méthane. Enfin, d’autres bactéries sulfato-réductrices (telles que Desulfovibrio, Bilophila ou Fusobacterium) utilisent le soufre pour produire du sulfure d’hydrogène (4).
Le schéma ci-dessous illustre ces trois profils principaux de déséquilibres microbiens, en mettant en évidence les types de micro-organismes impliqués et le gaz prédominant associé à chaque forme de SIBO. Ces distinctions sont importantes car elles influencent directement la symptomatologie digestive et la stratégie de prise en charge.

Dysbioses multiples : rétablir l’équilibre dans le bon ordre
Ces trois formes peuvent coexister simultanément. Lorsqu’elles sont présentes en même temps, il est essentiel de respecter un ordre précis dans la prise en charge : on commence par traiter l’ISO, puis l’IMO, et enfin le SIBO.
Il est également essentiel de garder à l’esprit que plus la charge microbienne en taxons perturbateurs est élevée, plus les symptômes cliniques seront marqués : douleurs, flatulences, alternances diarrhée/constipation, brouillard cérébral, intolérances alimentaires ou fatigue postprandiale. Cette corrélation traduit le fait qu’une production excessive de métabolites toxiques (gaz, acides organiques, amines biogènes) surcharge les capacités de détoxification et d’adaptation de l’hôte (5).
Comment diagnostiquer les différents types de SIBO ?
Le test respiratoire (breath test) au glucose ou au lactulose est actuellement la méthode la plus utilisée pour détecter un SIBO. Il repose sur la mesure sériée, toutes les 15 à 20 minutes, des gaz expirés après ingestion d’un substrat fermentescible. En situation normale, la fermentation bactérienne se produit dans le côlon ; une élévation précoce de l’un des gaz dans l’air expiré traduit donc une activité fermentaire anormale dans l’intestin grêle. Concernant le SIBO H2S, les tests respiratoires classiques ne détectent pas toujours ce gaz, mais de nouveaux dispositifs (tests trigas ou Trio-Smart®) permettent désormais de le mesurer simultanément à l’hydrogène et au méthane, améliorant la précision du diagnostic différentiel.
Même si les tests respiratoires restent la meilleure manière de confirmer et parfois de différencier les types de SIBO selon le gaz produit, le bilan clinique offre déjà de précieuses indications. En effet, la nature et la sévérité des symptômes orientent souvent vers un type de SIBO particulier. Ainsi, l’analyse fine des symptômes cliniques, mise en relation avec les données microbiologiques, permet souvent d’orienter le diagnostic avant même la confirmation par un test respiratoire.
L’interprétation des tests doit toujours être corrélée au tableau clinique et à d’éventuels facteurs favorisants (hypochlorhydrie, troubles du péristaltisme, prise chronique d’IPP, chirurgie digestive, etc.), afin d’orienter vers une prise en charge ciblée et personnalisée.
LISTE DES SYMPTÔMES PRINCIPAUX PAR TYPE DE CONFIGURATION :

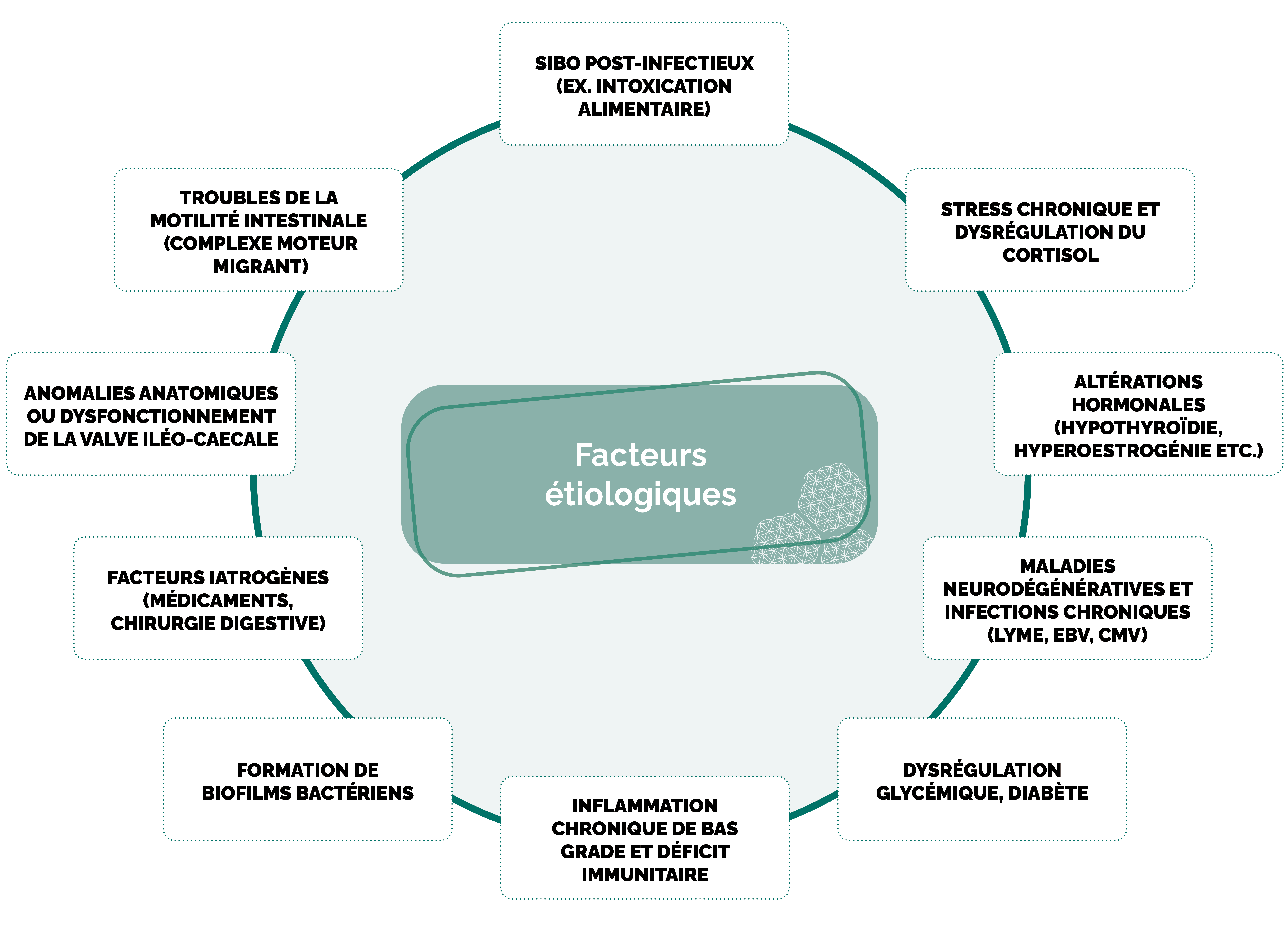
Les causes du SIBO
Les causes de l’apparition du SIBO sont multiples et intriquées. Bien que l’intoxication alimentaire soit souvent considérée comme un facteur déclencheur majeur, le développement d’un SIBO résulte le plus souvent d’une combinaison de déséquilibres qui favorisent la dysbiose intestinale.
Comme nous l’avons évoqué précédemment, l’ensemble du parcours digestif intervient dans le maintien de la santé et de la diversité du microbiote intestinal. Il est important de noter que le SIBO n’est pas une maladie en soit, ce phénomène est plutôt la conséquence d’un déséquilibre métabolique initial : digestion ralentie, hypothyroïdie, diabète, syndrome d’activation mastocytaire, charge virale froide, prise de médicaments, chirurgies etc.
Dans cette section, nous examinerons plus en détail certains des mécanismes et facteurs étiologiques susceptibles de favoriser la prolifération excessive de bactéries dans l’intestin grêle.
FOCUS SUR 4 CAUSES
Complexe moteur migrant (CMM)
Le CMM est un ensemble de contractions électromécaniques cycliques qui surviennent dans l’intestin grêle pendant les périodes de jeûne. Il agit comme un « balai intestinal », nettoyant le tube digestif des débris alimentaires, du mucus et des bactéries. Il s’active environ toutes les 90 à 120 min après le dernier repas et se déroule en trois phases :
- phase de repos,
- phase d’activité irrégulière,
- phase d’activité motrice intense et coordonnée qui progresse de l’estomac vers l’iléon.
Un CMM ralenti ou absent (notamment en phase 3, la plus purgative) favorise la stagnation du contenu intestinal et crée un environnement propice à la prolifération bactérienne dans l’intestin grêle et à l’hyperperméabilité intestinale. De nombreuses études montrent qu’un trouble du CMM est fréquemment observé chez les patients atteints de SIBO ou de troubles fonctionnels tels que le syndrome de l’intestin irritable (SII) (6).

Équilibre gastrique et enzymes digestives
Un bon fonctionnement gastrique, avec une sécrétion adéquate d’acide chlorhydrique, joue un rôle essentiel dans la dégradation des protéines et exerce une action antimicrobienne en éliminant ou en limitant la remontée de microbes vers l’intestin grêle. Une hypochlorhydrie affaiblit cette défense, laisse passer des microorganismes ou des substrats non digérés vers le grêle, et favorise ainsi les conditions propices à la fermentation et au SIBO (8).
Parallèlement, les enzymes digestives, produites en partie par le pancréas et en partie par la muqueuse intestinale, sont essentielles à la dégradation du bol alimentaire, mais aussi pour leurs propriétés antimicrobiennes et assainissantes. Cependant, il se peut que le fonctionnement enzymatique soit perturbé (hypothyroïdie, âge, dystonie neurovégétative, Helicobacter pylori, IPP etc.) et que ce processus soit altéré. L’apport exogène d’enzymes digestives permet de soulager le travail digestif et intestinal et par conséquent va réduire les substrats fermentescibles disponibles pour les bactéries dans l’intestin. Cela ne doit pas être considéré comme un remède en soi, mais une stratégie d’aide pour calmer et réduire l’inflammation intestinale et systémique.
Comme nous l’avons vu précédemment, l’intégralité du tube digestif doit être pris en considération, même si les problèmes ne se répercutent qu’au niveau de l’intestin grêle. En gardant cette notion en tête, il est important de se rappeler que l’usage prolongé des inhibiteurs de la pompe à protons (IPP) entraîne une perturbation chronique de l’acidité gastrique, et par conséquent impact le milieu intraluminal, affaiblit la barrière acide contre la remontée bactérienne (9).
Plusieurs méta-analyses ont montré que l’utilisation d’IPP était associée à un risque accru de SIBO (19 études, 7055 participants au total). De plus, chaque mois d’usage supplémentaire semblait augmenter le risque (10).
Dérèglements hormonaux
» Thyroïde, surrénales, hormones sexuelles
CORTISOL
Le stress chronique entraine une perturbation du cortisol et altère la signalisation vagale et la fonction entérique. Ce phénomène entraine un ralentissement de la motilité intestinale via une inhibition du système parasympathique et une diminution de la sécrétion gastrique et biliaire.
En outre, la stimulation parasympathique (via le nerf vague) est essentielle pour déclencher la sécrétion de Cholécystokinine (CCK) qui régule la libération d’enzymes pancréatiques et de bile.
Des études ont montré qu’un stress chronique élevé ou un hyperfonctionnement de l’axe hypothalamo-hypophyso-surrénalien peut altérer la motilité du grêle, la composition du microbiote intestinal et augmenter le nombre de taxons perturbateurs.
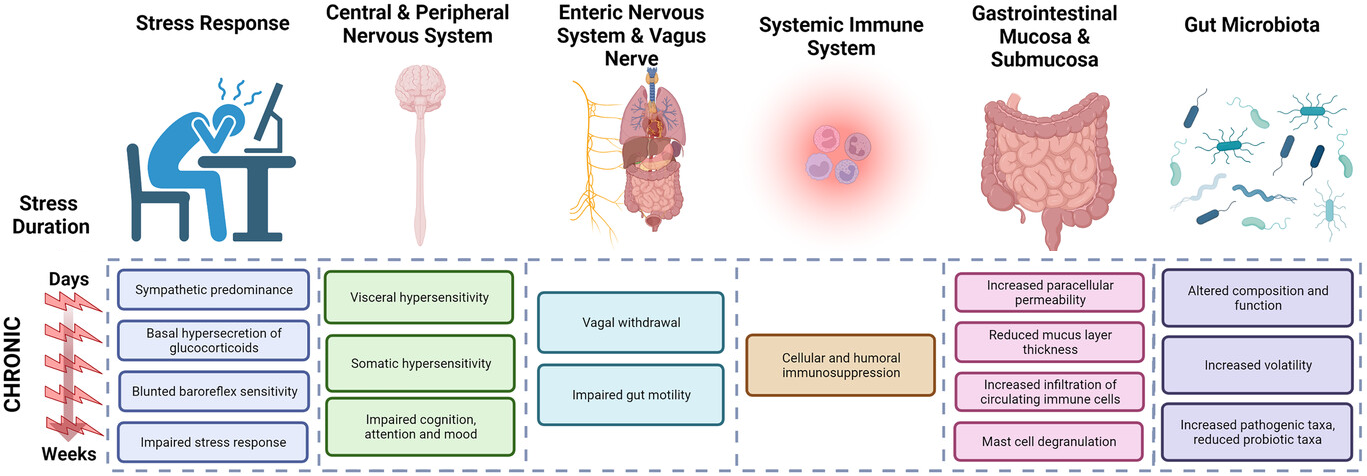
Source du schéma : Sarah-Jane Leigh et al. (2023). The impact of acute and chronic stress on gastrointestinal physiology and function: a microbiota–gut–brain axis perspective. J Physiol 601.20 (2023) pp 4491–4538.
L’HYPOTHYROIDIE
Les déséquilibres thyroïdiens, notamment l’hypothyroïdie, impactent fortement la fonction digestive et le microbiote intestinal. La motilité est altérée (ralentissement du transit, vidange gastrique retardée, dysfonction du complexe moteur migrant) et la régulation hormonale (gastrine, ghréline) perturbée, favorisant la stagnation du contenu intestinal et créant un terrain propice au SIBO et à la dysbiose.
Sur le plan métabolique, l’hypothyroïdie réduit la production d’acides biliaires secondaires, diminuant leur effet antimicrobien dans le grêle. Elle s’accompagne également d’une baisse de la diversité bactérienne, d’une moindre production d’acides gras à chaîne courte (butyrate) et d’un déséquilibre Firmicutes/Bacteroidetes, contribuant à la perméabilité intestinale et à l’activation du système immunitaire (TLR4, Th1/Th2) (11).
Ainsi, un cercle vicieux s’installe : la dysfonction thyroïdienne altère le microbiote et ses métabolites, ce qui entretient l’inflammation et favorise les maladies auto-immunes thyroïdiennes, comme la thyroïdite de Hashimoto. L’axe thyroïde–intestin–immunité repose donc sur des interactions métaboliques complexes où chaque dysfonction amplifie l’autre.
Relation entre dysbiose et dysfonctionnement thyroïdien
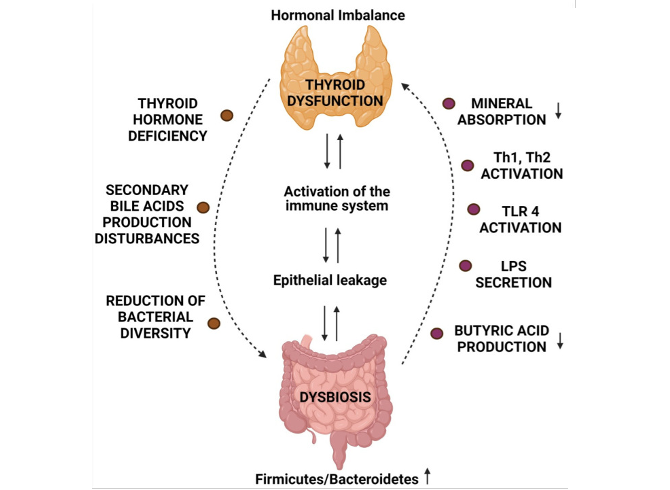
Source du schéma : Piotr Bargiel et al. (2021). Microbiome Metabolites and Thyroid Dysfunction. J Clin Med. 2021 Aug
Infections virales chroniques
(12) (13) (14)
Les infections virales chroniques ou les réactivations virales latentes (comme certains entérovirus, cytomégalovirus, EBV, HSV, HHV-6) peuvent influencer la physiopathologie du SIBO de manière indirecte mais significative. Ces virus ont la capacité d’induire une inflammation de bas grade persistante, une altération de la barrière épithéliale, un changement du microbiote, et une perturbation du fonctionnement thyroïdien et du système nerveux entérique.
Cette inflammation soutenue favorise la dysrégulation des jonctions serrées entre entérocytes, accroît la perméabilité intestinale (« leaky gut »), et facilite la translocation de fragments bactériens ou de lipopolysaccharides dans la circulation. Cette situation entraîne un cercle vicieux : la barrière altérée permet un contact accru entre les antigènes microbiens et le système immunitaire, ce qui entretient l’inflammation, module négativement la composition du microbiote et peut contribuer à des troubles intestinaux fonctionnels, à des déséquilibres immunitaires (augmentation de la prévalence de maladie auto-immune) et à des manifestations systémiques.
Les champignons adaptogènes riches en polysaccharides (β-glucanes) (le Reishi, le Cordyceps, l’hydne herisson ou le Chaga) et la racine d’astragale exercent plusieurs effets biologiques susceptibles de soutenir la fonction digestive, la motilité et la régulation immunitaire dans un contexte de SIBO associé à une charge virale chronique.
→ Découvrir IMU-MICO
APPROCHES NATURELLES DANS L’ACCOMPAGNEMENT DU SIBO
L’importance de la santé buccale
La santé buccale dépasse la simple hygiène dentaire : elle influence l’écologie microbienne de tout le tube digestif. Des études ont montré que certaines bactéries orales, comme les Streptococcus, peuvent transiter vers l’intestin et s’y implanter. Par exemple, chez des patients atteints de maladies inflammatoires de l’intestin (MICI), des souches identiques ont été retrouvées dans la salive et les selles, suggérant une colonisation ectopique (15).
Cet « axe bouche‑intestin » a des implications physiopathologiques : l’arrivée de germes oraux dans le grêle peut favoriser une surpopulation bactérienne non adaptée (SIBO), altérer la barrière muqueuse et déclencher une inflammation. Chez des patients IBS-D, la diversité du microbiote lingual est réduite, avec surreprésentation de Veillonella et Prevotella et diminution de Streptococcus, Haemophilus, Rothia et Granulicatella (16).
Selon ses données, les résultats indiquent que le microbiote buccal peut contribuer activement à la dysbiose intestinale. Une mauvaise hygiène buccale, une dysbiose linguale ou la prolifération de certaines espèces orales peuvent ainsi favoriser ou entretenir un SIBO (17).
Low-FODMAP vs bi-phasic
» Quelle stratégie choisir ?
Dans la prise en charge du SIBO, il est important de distinguer le régime low-FODMAP du régime bi-phasic. Le régime low-FODMAP se concentre sur la réduction des symptômes digestifs en limitant les glucides fermentescibles, sans agir directement sur la prolifération bactérienne. À l’inverse, le régime bi-phasic, spécifiquement conçu pour le SIBO, se déroule en deux étapes : une phase initiale stricte destinée à « affamer » la flore bactérienne de l’intestin grêle en limitant fortement les substrats fermentescibles, suivie d’une phase de réintroduction progressive des aliments tolérés.
Cette méthode permet non seulement un soulagement rapide des symptômes, mais constitue également une stratégie pour diminuer le risque de récidive et favoriser le rééquilibrage du microbiote. Contrairement au low-FODMAP, elle cible la physiopathologie du SIBO et offre une approche dépassant le simple soulagement symptomatique.
Zoom sur certains actifs
Argent colloïdal
» un outil précieux dans une stratégie intégrative.
L’argent colloïdal, en particulier sous forme de nanoparticules, est aujourd’hui reconnu comme un antiseptique buccal intéressant, capable d’agir de manière ciblée sur l’ensemble du microbiote oral. Les ions argent exercent une action antimicrobienne multiforme à large spectre, ce qui en fait un agent particulièrement performant pour assainir la sphère orale.
Plusieurs essais cliniques ont démontré que les bains de bouche contenant des nanoparticules d’argent (AgNPs) réduisent efficacement la plaque dentaire, les populations de Streptococcus mutans — l’une des bactéries majeures impliquées dans les dysbioses buccales — ainsi que les marqueurs d’inflammation gingivale. Dans certaines études (18), leur efficacité est équivalente à celle de la chlorhexidine, tout en offrant une meilleure tolérance et sans induire de coloration dentaire. Ces résultats montrent que l’argent colloïdal constitue une alternative moderne, naturelle et performante.
- Une action déterminante sur le biofilm buccal, clé de la prévention des réinfections digestives.
Au-delà de la simple réduction des bactéries libres, les formulations à base d’argent présentent un avantage majeur : leur capacité à désorganiser le biofilm buccal. Ce biofilm — véritable « réservoir » microbien — joue un rôle central dans les rechutes récurrentes de dysbioses digestives, y compris dans certains cas de SIBO où la source d’inoculation provient de la cavité orale. En diminuant la cohésion du biofilm et en réduisant la densité bactérienne pathogène, l’argent colloïdal contribue à limiter les recolonisations répétées du tube digestif, en particulier dans les contextes où des bactéries d’origine orale migrent vers l’intestin grêle (19).
Hericium erinaceus
L’hericium erinaceus est un champignon riche en polysaccharides et en composés bioactifs qui modulent le microbiote intestinal, réduisent l’inflammation et améliorent le stress oxydatif.
Il possède des effets anti-inflammatoires, notamment l’inhibition de la signalisation NF-kB et la modulation des cytokines. Il est reconnu pour ses propriétés neuroprotectrices, favorisant la neurorégération.
L’hericium soutient le développement de plusieurs bactéries bénéfiques, notamment les Bifidobacterium, Lactobacillus, Roseburia, Blautia, Anaerostipes, Sutterella, Desulfovibrio, tout en réduisant la prolifération de bactéries potentiellement pathogènes (20).
Cette modulation diminue la production d’endotoxines, notamment le LPS (lipopolysaccharides), contribuant ainsi à réduire l’inflammation systémique et les perturbations microcirculatoires. Ces mécanismes sont particulièrement pertinents en cas de SIBO, où la perméabilité intestinale et la dysfonction du réseau nerveux entérique (incluant le nerf vague) peuvent jouer un rôle dans la symptomatologie.
Baume antique de Jérusalem
Le Baume antique de Jérusalem est un élixir traditionnel très ancien, utilisé depuis des siècles au Moyen-Orient et en Europe.
Sa formule associe la myrrhe (guggul), l’encens (boswellia), l’aloe vera, le mastic (lentisque pistachier) et la menthe poivrée, qui exercent des actions synergiques sur tout le tube digestif. Il est connu pour ses propriétés anti-inflammatoires, antimicrobiennes, antioxydantes et protectrices digestives.
Il est particulièrement recommandé pour faciliter la vidange gastrique et pour aider à réparer la muqueuse gastrique et comme anti-inflammatoire de bas gras grade d’origine intestinale, ce qui en fait un remède précieux dans le cadre du SIBO et de la colopathie fonctionnelle.
Butyrate
Le butyrate est un acide gras à chaîne courte (AGCC) produit naturellement dans le côlon par la fermentation des fibres alimentaires par le microbiote intestinal. Il joue un rôle clé dans la santé digestive et métabolique. Il s’agit d’un postbiotique, c’est-à-dire un métabolite bioactif produit par les bactéries intestinales qui exerce des effets bénéfiques directs sur l’hôte, indépendamment de la présence de bactéries vivantes.
Le butyrate est métabolisé par les mitochondries en tant que source d’énergie (ATP) pour les cellules du côlon. Dans le SIBO, la dysbiose et l’appauvrissement en bactéries productrices d’acides gras à chaînes courtes (et donc en butyrate) peuvent contribuer à une perméabilité muqueuse accrue, une inflammation locale et une altération de la motilité. Des études de microbiote montrent une réduction des AGCC (dont le butyrate) en contexte de déséquilibre alimentaire et de dysbiose intestinale. Sur le plan clinique, des formes micro-encapsulées de butyrate oral ont été testées et rapportent des améliorations des symptômes gastro-intestinaux (ballonnements, diarrhée/constipation, douleurs abdominales, nausées, vomissement, gazs) et des marqueurs de SIBO (21).
Le butyrate peut être envisagé comme une aide dans le SIBO pour restaurer la trophicité épithéliale, diminuer l’inflammation muqueuse et améliorer la motilité intestinale.

Suggestions de protocoles



Références bilbliographiques :
(1) Leite, G., Rezaie, A., Mathur, R., Barlow, G. , Rashid, M., Hosseini, A., Wang, J., Parodi, G., Villanueva‑Millán, M. J., Sanchez, M., Morales, W., Weitsman, S., & Pimentel, M. (2024). Defining Small Intestinal Bacterial Overgrowth by Culture and High Throughput Sequencing. Clinical Gastroenterology and Hepatology, 22(2), 259‑270.
(2) Li, J., Wang, J., Zhang, R., et al. (2021). Mucosa-Associated Microbial Profile Is Altered in Small Intestinal Bacterial Overgrowth. Frontiers in Microbiology, 12, 710940.
(3) Jacob T Barlow et al. Quantitative sequencing clarifies the role of disruptor taxa, oral microbiota, and strict anaerobes in the human small-intestine microbiome. 2021 Nov 2; 9:214.
(4) Taojun Wang et al. In vitro interactions between Blautia hydrogenotrophica, Desulfovibrio piger and Methanobrevibacter smithii under hydrogenotrophic conditions. Gut Microbes. 2023 Sep 27;15(2):2261784.
(5) Christian Boyer, Mai 2024, Le SIBO ou pullulation bactérienne de l’intestin grêle, blog de Dyjest, https://blog.dyjest.care/posts/sibo-part-1/
(6) Mark Pimentel et al. Lower Frequency of MMC Is Found in IBS Subjects with Abnormal Lactulose Breath Test, Suggesting Bacterial Overgrowth. Digestive Diseases and Sciences, Vol. 47, No. 12 (2002), pp. 2639–2643.
(7) Mehrnaz Nikkhah Bodaghet al.(2018). Ginger in gastrointestinal disorders: A systematic review of clinical trials. Food Sci Nutr. 2018 Nov 5;7(1):96–108.
(8) Andrew C. Dukowicz et al. (2007). Small Intestinal Bacterial Overgrowth: A Comprehensive Review. Gastroenterology & Hepatology Volume 3, Issue 2.
(9) Tingting Su et al. (2017). Meta-analysis: proton pump inhibitors moderately increase the risk of small intestinal bacterial overgrowth. J Gastroenterol. 2018 Jan;53(1):27-36.
(10) Alsu R Khurmatullina (2025). The Duration of Proton Pump Inhibitor Therapy and the Risk of Small Intestinal Bacterial Overgrowth: A Systematic Review and Meta-Analysis. J Clin Med. 2025 Jul 3;14(13):4702.
(11) Xu, G.-M., Hu, M.-X., Li, S.-Y., Ran, X., Zhang, H., & Ding, X.-F. (2024). Thyroid disorders and gastrointestinal dysmotility: An old association. Frontiers in Physiology, 15, Article 1389113.
(12) Ceylan Tanes et al. (2021). Gut Microbiome Changes Associated with Epithelial Barrier Damage and Systemic Inflammation during Antiretroviral Therapy of Chronic SIV Infection. 2021 Aug 8;13(8):1567.
(13) Antonella Gallo et al. (2025). Intestinal Inflammation and Permeability in Patients Recovered from SARS-CoV-2 Infection. Dig Dis. 2025;43(1):1-10.
(14) Zachary J. Morse et al. (2021). Virus Infection Is an Instigator of Intestinal Dysbiosis Leading to Type 1 Diabetes. Immunol., Sec. Immunological Tolerance and Regulation, Volume 12.
(15) Kitamoto, S., Nagao-Kitamoto, H., Hein, R., Schmidt, T. M., & Kamada, N. (2020). The Bacterial Connection between the Oral Cavity and the Gut Diseases. Journal of Dental Research, 99(9), 1021-1029.
(16) Li, Y., Mai, Y., Jiao, Y., Yuan, Y., Qu, Y., Zhang, Y., Wang, M., Zhang, W., Lu, X., Lin, Z., Li, J., Mao, T., & Xie, C. (2025, février). Alterations in the tongue coating microbiome in patients with diarrhea-predominant irritable bowel syndrome: A cross-sectional study. APMIS, 133(2), e70001.
(7) Abdelbary, M. M. H., Hommola, A. K., Diederichs, A., Knueppel, L., Bode, A., Depner, M., … & Ott, S. (2022). The oral-gut axis: Salivary and fecal microbiome dysbiosis in inflammatory bowel disease. Frontiers in Cellular and Infection Microbiology, 12, Article 1010853.
(18) Thao, D. T., Nguyen Thi, Y. H., Le Nguyen, D. H., Dang The, A. T., Tru Nguyen, C. P., Nguyen, V. T., Quach, U. N., & Truong, L. T. (2025). Comparing the Effectiveness of 0.12% Chlorhexidine and Silver Nanoparticles Mouthwashes: A Double-Blind Randomized Controlled Trial Among Medical Students in Southern Vietnam. Cureus, 17(7), e87948.
(19) Raghav, P., Khera, A. , & Bisht, S. (2025). Comparative evaluation of antimicrobial properties of silver nanoparticles and chlorhexidine mouthwashes on the colonization of microflora and oral health during orthodontic treatment: A double‑blind randomized controlled trial. Dental Press Journal of Orthodontics, 30(1), e2524112.
(20) Miaoyu Li et al. (2021). Role of dietary edible mushrooms in the modulation of gut microbiota. Journal of Functional Foods 83 (2021) 104538.
(21) George B. Saffouri et al. (2019) Small intestinal microbial dysbiosis underlies symptoms associated with functional gastrointestinal disorders. Nature communications (2019) 10:2012.
Document réservé à l’usage des praticiens de santé.
