
INLEIDING
SIBO, of bacteriële overgroei van de dunne darm, is een bekende aandoening, maar het onderzoek naar de werking ervan – en naar de darm in zijn geheel wordt steeds nauwkeuriger. Deze nieuwe inzichten helpen de complexiteit ervan beter te begrijpen, de onderliggende oorzaken en de impact van een verstoring op het hele spijsverteringsstelsel.
In tegenstelling tot de dikke darm, de natuurlijke plaats van fermentatie, is de dunne darm een orgaan van opname. Wanneer deze een plaats van fermentatie wordt, ontstaan de eerste symptomen: een opgeblazen gevoel, pijn en spijsverteringsklachten.
Om SIBO te begrijpen, moet het in de context van het gehele spijsverteringsstelsel worden geplaatst: mond, maag, lever, alvleesklier, darmen… elk orgaan werkt als een schakel in een keten, en een verstoring kan het hele systeem uit balans brengen.
Laten we samen de nieuwste wetenschappelijke inzichten en integratieve oplossingen voor de verschillende vormen van SIBO bekijken: H₂, CH₄ en H₂S. Een globale benadering is noodzakelijk om deze aandoening te begrijpen, het evenwicht te herstellen en de spijsvertering op een doeltreffende manier te ondersteunen!
Fysiopathologie van SIBO
In normale omstandigheden blijft de bacteriële concentratie in de dunne darm zeer laag, minder dan 10³ eenheden per milliliter, waardoor fermentatie wordt beperkt en de integriteit van het slijmvlies behouden blijft. Bij SIBO, is deze regulering verstoord: de overmatige verspreiding van bacteriën lijdt tot voortijdige fermentatie van suikers en de productie van gassen (waterstof, methaan, waterstofsulfide).
Deze gasvormige metabolieten oefenen mechanische en biochemische druk uit op een slecht aangepast slijmvlies, wat de hyperpermeabiliteit van de darm bevordert. De verhoogde blootstelling van de darmbarrière aan endotoxinen en bacteriële fragmenten veroorzaakt vervolgens een lichte ontsteking en een chronische immuun-activatie, wat bijdraagt aan de spijsverteringssymptomen (opgeblazen gevoel, pijn, diarree of constipatie) en systemische symptomen van SIBO.
Op lange termijn kan dit leiden tot een ernstige slechte opname van voedingsstoffen, voornamelijk koolhydraten, vetten, eiwitten en ijzer, wat kan leiden tot voedingstekorten en ondervoeding of de ontwikkeling van andere aandoeningen zoals obesitas, coeliakie, prikkelbare darmsyndroom, leverschade, enz.
Functioneel onderscheid: dunne darm vs. dikke darm
Hoewel ze vaak onterecht onder één en dezelfde spijsverteringsaanpak worden geplaatst, hebben de dikke darm en de dunne darm zeer verschillende functies. De dunne darm is in de eerste plaats een plaats van verwerking: zijn wanden zijn doorlaatbaarder en rijkelijk doorbloed, waardoor essentiële voedingsstoffen kunnen worden opgenomen. die kleiner maar zeer gespecialiseerd is, speelt een rol bij de vertering, de regulering van het immuunsysteem en het metabolisme van voedingsstoffen.
De dikke darm daarentegen is een gebied waar fermentatie plaatsvindt. De omgeving is hier dichter van slijm en bacteriën, wat de afbraak van onverteerde vezels en de productie van heilzame korteketenvetzuren bevordert.
De darmflora en de dunne darmflora (SIB) reageren op zeer verschillende evenwichtssituaties: elk verdient een specifieke aanpak, zowel wat betreft het begrijpen van de functies ervan als wat betreft de strategieën om het evenwicht te herstellen.
Wijzigingen in microbiële netwerken
Bovenop de eenvoudige bacteriële overgroei gaat SIBO gepaard met een grondige ontregeling van het microbiële netwerk van het duodenum (1). De symbiotische wisselwerkingen die zorgen voor de verbinding, communicatie en functionele regulering van microbiële gemeenschappen worden verstoord. Dit verlies aan verbinding beïnvloedt de productie van gunstige metabolieten, de modulatie van de lokale immuunrespons en de optimale vertering van voedingsstoffen.
De ontregeling van deze netwerken bevordert het ontstaan van opportunistische stammen ten koste van belangrijke symbioten, waardoor de functionele verscheidenheid afneemt en de onstabiliteit van het darm-ecosysteem toeneemt (2). Meer nog dan het verlies aan verscheidenheid zelf, is het deze verstoring van de microbiële communicatie die de klinische complexiteit van SIBO verklaart en een globale therapeutische aanpak rechtvaardigt die gericht is op het herstel van het ecologisch evenwicht en de microbiële veerkracht.
Het volledige spijsverteringsproces overwegen
SIBO kan niet op zichzelf worden begrepen: het is een weerspiegeling van een algehele disbalans in het spijsverteringsstelsel en elke stap in het proces, van de mond tot de dikke darm, speelt een belangrijke rol bij het voorkomen of verergeren ervan.
De maag en zijn zuurgraad beperken de opname van ongewenste microben. Gal en pancreasenzymen helpen bij de afvoer ervan en zorgen tegelijkertijd voor de vertering. Het motorische migratiecomplex reinigt de darm tussen de maaltijden door, terwijl de Klep van Bauhin voorkomt dat bacteriën uit de dikke darm omhoog komen. Ten slotte, zorgt het darmimmuunsysteem voor het algemene evenwicht van de microbiota.
Wanneer één van deze schakels verzwakt, raakt het hele proces ontregeld, waardoor de dunne darm, die een plaats van verwerking is, verandert in een plaats van gisting.
SIBO begrijpen betekent dus de spijsvertering overwegen als een logisch geheel waarin elk orgaan zijn rol speelt in het evenwicht.
Onderscheid maken om beter te kunnen behandelen
- SIBO (Small Intestinal Bacterial Overgrowth) is een overmatige groei van pathogene bacteriën in de dunne darm (jejunum of ileum), waarbij het aantal bacteriën hoger is dan 10⁵ CFU/mL. Dit gaat vaak gepaard met een verarming van de microbiota en een verstoring van het microbiële evenwicht.
- SIFO (Small Intestinal Fungal Overgrowth) duidt op een schimmelovergroei, meestal van Candida-soorten, ter hoogte van de dunne darm.
- LIBO (Large Intestinal Bacterial Overgrowth) betreft de dikke darm, met een verstoorde darmflora en vaak een verhoogde methaanproductie.
- IBS (het prikkelbare darmsyndroom) een functionele aandoening die wordt gekenmerkt door buikpijn en verstoringen van de darmtransit, meestal zonder duidelijk geïdentificeerde microbiële overgroei.

ZOOM OP SIBO
De drie gezichten van SIBO
Dankzij wetenschappelijke vooruitgang kunnen onevenwichtigheden in de darmflora nu echter beter worden gekarakteriseerd en kunnen drie hoofdconfiguraties worden onderscheiden op basis van het type gas dat wordt geproduceerd: SIBO waterstof (H₂), SIBO methaan (CH₄) en SIBO waterstofsulfide (H₂S).
Deze vormen zijn afhankelijk van de aanwezigheid en de verspreiding van “microbiële hormoonverstoorder”, die tijdens de fermentatie van voedingssubstraten verschillende gassen kunnen produceren (3).
Zo produceren bepaalde bacteriën (zoals E. coli of Klebsiella) voornamelijk waterstof, terwijl methanogene archaea (zoals Methanobrevibacter smithii) deze waterstof omzetten in methaan. Ten slotte gebruiken andere sulfaatreducerende bacteriën (zoals Desulfovibrio, Bilophila of Fusobacterium) zwavel om waterstofsulfide te produceren (4).
Het onderstaande schema illustreert deze drie hoofdprofielen van microbiële onevenwichtigheden, door de soorten micro-organismen die hierbij betrokken zijn en het gas dat bij elke vorm van SIBO overheerst, te benadrukken. Deze verschillen zijn belangrijk omdat ze een directe invloed hebben op de spijsverteringssymptomen en de behandelingsstrategie.

Meervoudige dysbiose: het evenwicht in de juiste volgorde herstellen
Deze drie vormen kunnen tegelijkertijd voorkomen. Wanneer ze tegelijkertijd aanwezig zijn, is het belangrijk om een bepaalde volgorde aan te houden bij de behandeling: eerst wordt ISO behandeld, daarna IMO en ten slotte SIBO.
Het is ook belangrijk om te onthouden dat hoe hoger de microbiële belasting aan hormoonverstoorders, hoe ernstiger de klinische symptomen zullen zijn: buikpijn, winderigheid, afwisselend tussen diarree/ constipatie, hersenmist, voedselintoleranties of vermoeidheid na de maaltijd. Deze correlatie weerspiegelt het feit dat een overmatige productie van toxische metabolieten (gassen, organische zuren, biogene aminen) de ontgiftings- en aanpassingscapaciteit van de gastheer overbelast (5).
Hoe worden de verschillende types SIBO gediagnosticeerd?
De glucose-of lactulose- ademtest (breath test) is momenteel de meest gebruikte methode om SIBO op te sporen. Deze test is gericht op het meten van de uitgeademde gassen na inname van een fermenteerbaar substraat, om de 15 tot 20 minuten. In normale omstandigheden vindt bacteriële fermentatie plaats in de dikke darm; een vroege stijging van één van de gassen in de uitgeademde lucht duidt dus op abnormale fermentatieactiviteit in de dunne darm. Wat SIBO H2S betreft, detecteren klassieke ademhalingstests dit gas niet altijd, maar met nieuwe apparaten (trigas-test of Trio-Smart®) kan het nu tegelijk met waterstof en methaan worden gemeten, wat de nauwkeurigheid van de verschillende diagnoses verbetert.
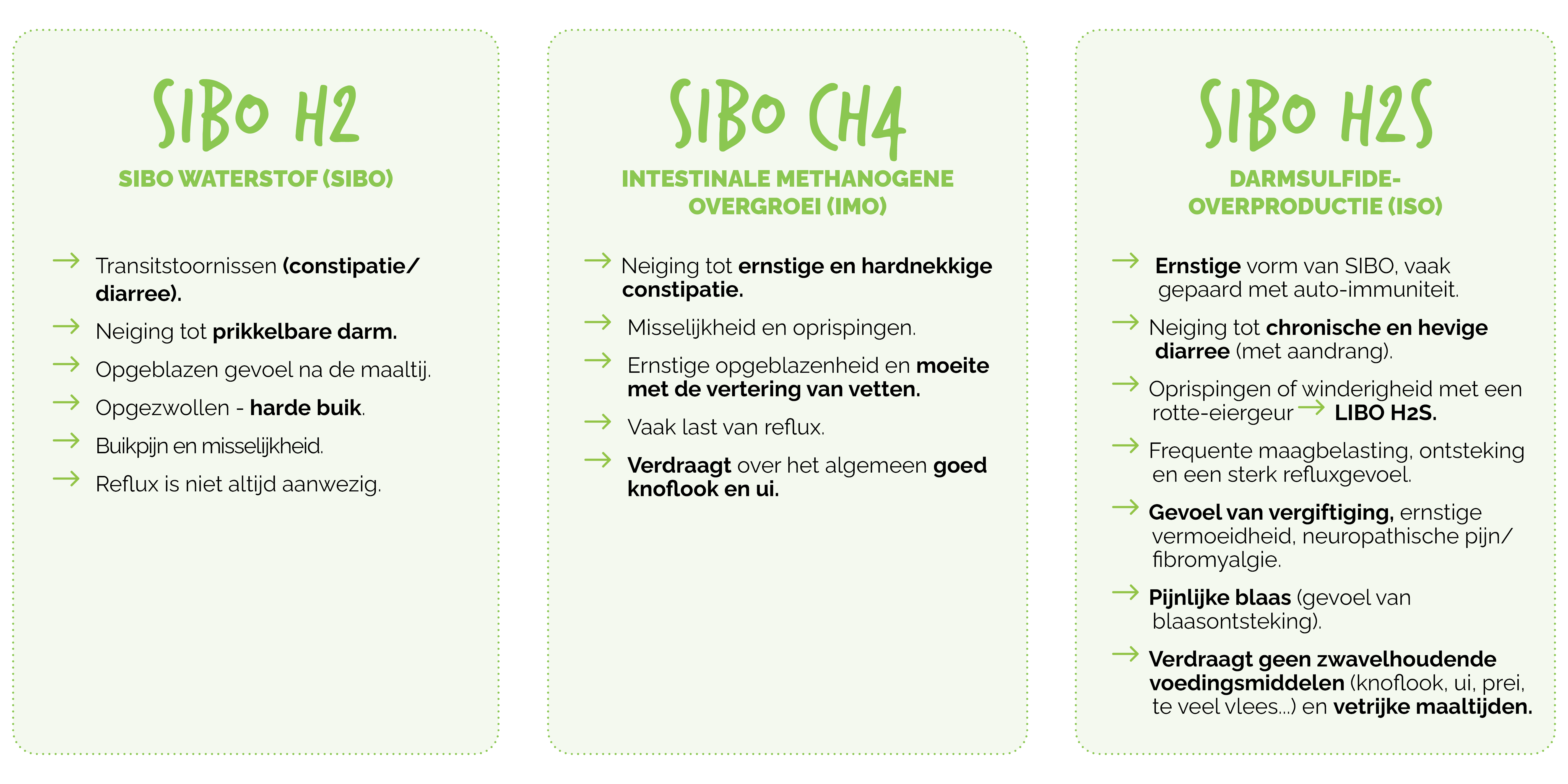
Hoewel ademhalingstests nog steeds de beste manier zijn om SIBO te bevestigen en soms te onderscheiden op basis van het geproduceerde gas, biedt het klinisch onderzoek al waardevolle aanwijzingen. De aard en ernst van de symptomen wijzen namelijk vaak op een bepaald type SIBO. Een grondige analyse van de klinische symptomen, in combinatie met microbiologische gegevens, maakt het dus vaak mogelijk om de diagnose te stellen nog voordat deze door een ademtest wordt bevestigd.
De resultaten van de tests moeten altijd worden beoordeeld in samenhang met het klinische beeld en eventuele bevorderende factoren (hypochlorhydrie, peristaltische stoornissen, chronisch gebruik van PPI’s, maag-darmchirurgie, enz.), om een gerichte en gepersonaliseerde behandeling te kunnen voorschrijven.
OVERZICHT VAN DE BELANGRIJKSTE SYMTOMEN PER TYPE CONFIGURATIE:
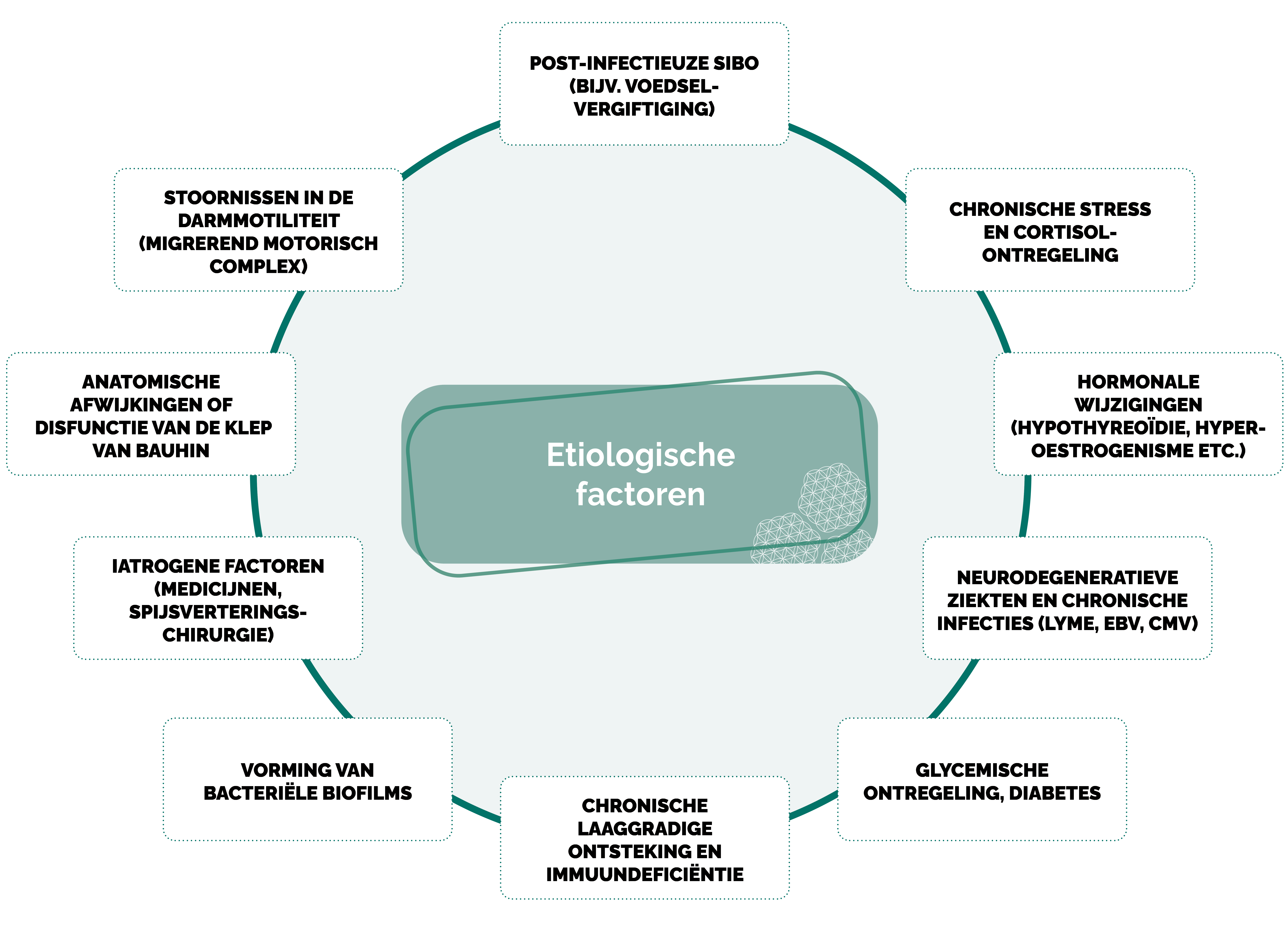
De oorzaken van SIBO
De oorzaken van SIBO zijn talrijk en complex. Hoewel voedselvergiftiging vaak wordt beschouwd als een belangrijke oorzaak, is de ontwikkeling van SIBO meestal het gevolg van een combinatie van onevenwichtigheden die darmdysbiose bevorderen.
Zoals eerder vermeld, speelt het hele spijsverteringsstelsel een rol bij het behoud van de gezondheid en diversiteit van de darmmicrobiota. Het is belangrijk op te merken dat SIBO op zich geen ziekte is, maar eerder het gevolg van een aanvankelijke metabolische disbalans: vertraagde spijsvertering, hypothyreoïdie, diabetes, mestcelactiveringssyndroom, koude virusbelasting, medicijngebruik, operaties enz.
In dit deel gaan we dieper in op enkele mechanismen en etiologische factoren die de overmatige toename van bacteriën in de dunne darm kunnen bevorderen.
FOCUS OP 4 OORZAKEN
Het migrerend motorisch complex (MMC)
Het MMC is een reeks cyclische elektromechanische contracties die tijdens periodes van vasten in de dunne darm plaatsvinden. Het werkt als een « darmbezem », en reinigt het spijsverteringskanaal van voedselresten, slijm en bacteriën. Het wordt ongeveer elke 90 tot 120 minuten na de laatste maaltijd geactiveerd en verloopt in drie fasen:
- rustfase,
- fase van onregelmatige activiteit,
- fase van intense en gecoördineerde motorische activiteit die zich van de maag naar de kronkeldarm uitbreidt.
Een vertraagde of afwezige MMC (in het bijzonder in fase 3, de meest laxerende fase) bevordert de stagnering van de darminhoud en zorgt voor een omgeving die bevorderlijk is voor bacteriële verspreiding in de dunne darm en voor darmhyperpermeabiliteit. Talrijke studies tonen aan dat een CMM-stoornis vaak wordt waargenomen bij patiënten met SIBO of functionele stoornissen zoals het prikkelbare darm syndroom. (SII) (6).

Maagbalans en spijsverteringsenzymen
Een goede maagfunctie, met een voldoende afscheiding van zoutzuur, speelt een belangrijke rol bij de afbraak van eiwitten en heeft een antimicrobiële werking door het verwijderen of beperken van het opstijgen van microben naar de dunne darm. Hypochlorhydrie verzwakt deze afweer, laat micro-organismen of onverteerde substraten door naar de dunne darm en bevordert zo de omstandigheden die gunstig zijn voor fermentatie en SIBO (8).
Daarentegen zijn de spijsverteringsenzymen, die deels door de alvleesklier en deels door het darmslijmvlies worden geproduceerd, belangrijk voor de afbraak van voedsel, maar ook vanwege hun antimicrobiële en reinigende eigenschappen. Het kan echter voorkomen dat de enzymatische werking verstoord is (hypothyreoïdie, leeftijd, neurovegetatieve dystonie, Helicobacter pylori, PPI enz.) en dat dit proces verstoord is. De exogene toevoer van spijsverteringsenzymen verlicht het werk van de spijsvertering en de darmen en vermindert daardoor de fermenteerbare substraten die beschikbaar zijn voor bacteriën in de darmen. Dit mag niet als een oplossing op zich worden beschouwd, maar als een strategie om darm- en systemische ontstekingen te kalmeren en te verminderen.
Zoals we eerder hebben gezien, moet rekening worden gehouden met het gehele spijsverteringskanaal, zelfs als de problemen zich alleen in de dunne darm voordoen. Met dit in gedachten is het belangrijk om te onthouden dat langdurig gebruik van protonpompremmers (PPI’s) leidt tot een chronische verstoring van de maagzuurgraad, wat vervolgens invloed heeft op het intraluminale milieu en de zuurbarrière tegen bacteriële reflux verzwakt (9).
Verschillende meta-analyses hebben aangetoond dat het gebruik van PPI’s gepaard gaat met een verhoogd risico op SIBO (19 onderzoeken, in totaal 7055 deelnemers). Bovendien leek elke extra maand gebruik het risico te verhogen (10).
Hormonale stoornissen
» Schildklier, bijnieren, geslachtshormonen
CORTISOL
Chronische stress leidt tot een verstoring van cortisol en beïnvloedt de vagale signalering en de darmslag. Dit fenomeen leidt tot een vertraging van de darmmotiliteit door een remming van het parasympathische systeem en een afname van de maag- en galafscheiding.
Bovendien is parasympathische stimulatie (via de nervus vagus) noodzakelijk om de afscheiding van cholecystokinin (CCK) op gang te brengen, dat de afgifte van pancreasenzymen en gal reguleert.
Onderzoek heeft aangetoond dat chronische stress of een overactieve hypothalamus-hypofyse-bijnieras de motiliteit van de dunne darm en de samenstelling van de darmflora kan verstoren en het aantal hormoonverstoorders kan doen toenemen.
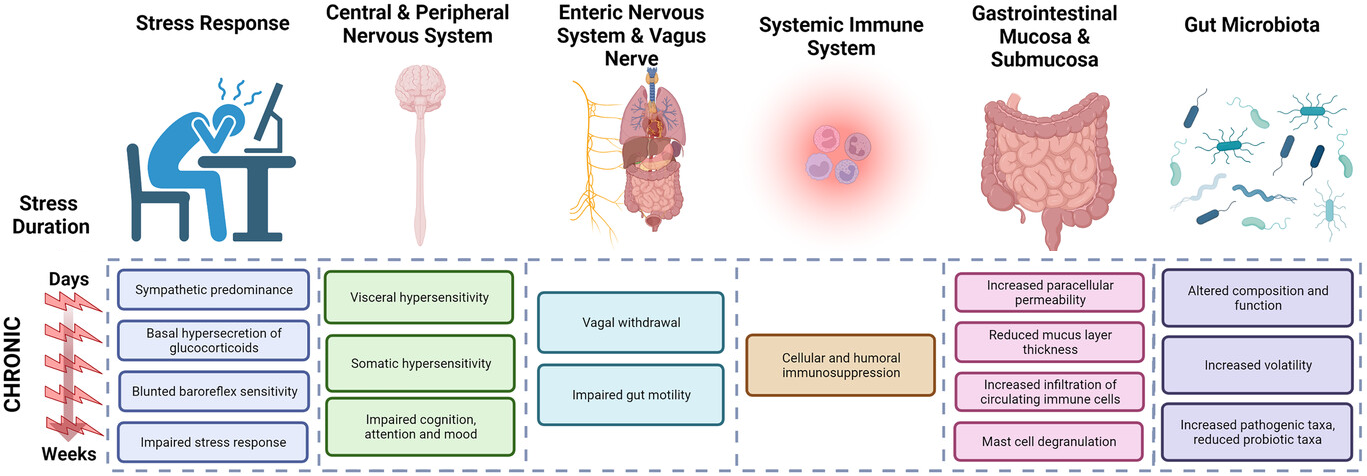
Bron van de schema : Sarah-Jane Leigh et al. (2023). The impact of acute and chronic stress on gastrointestinal physiology and function: a microbiota–gut–brain axis perspective. J Physiol 601.20 (2023) pp 4491–4538.
HYPOTHYROIDIE
Schildklierstoornissen, zoals hypothyreoïdie, hebben een grote invloed op de spijsvertering en de darmflora. De motiliteit wordt verstoord (vertraagde darmtransit, vertraagde maaglediging, disfunctie van het migrerende motorische complex) en de hormonale regulatie (gastrine, ghreline) wordt verstoord, wat stagnatie van de darminhoud bevordert en een gunstige voedingsbodem vormt voor SIBO en dysbiose.
Op metabolisch vlak vermindert hypothyreoïdie de productie van secundaire galzuren, waardoor hun antimicrobiële werking in de dunne darm afneemt. Het gaat ook gepaard met een afname van de bacteriële diversiteit, een verminderde productie van korteketenvetzuren (butyraat) en een verstoring van het evenwicht tussen Firmicutes en Bacteroidetes, wat bijdraagt aan de darmpermeabiliteit en de activering van het immuunsysteem (TLR4, Th1/Th2) (11).
Zo ontstaat een duivelskring: de schildklierdisfunctie verandert de microbiota en zijn metabolieten, wat de ontsteking in stand houdt en auto-immuunziekten van de schildklier, zoals Hashimoto-thyroïditis, bevordert. De schildklier-darm-immuniteitsas is dus gebaseerd op complexe metabolische interacties waarbij elke disfunctie de andere versterkt.
Verband tussen dysbiose en schildklierdisfunctie
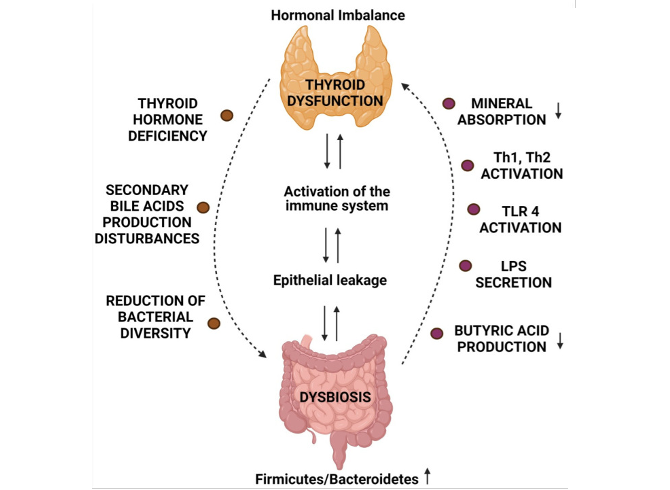
Bron van de schema : Piotr Bargiel et al. (2021). Microbiome Metabolites and Thyroid Dysfunction. J Clin Med. 2021 Aug.
Chronische virale infecties
(12) (13) (14)
Chronische virale infecties of latente virale reactiveringen (zoals bepaalde enterovirussen, cytomegalovirus, EBV, HSV, HHV-6) kunnen de pathofysiologie van SIBO op onrechtstreekse maar significante wijze beïnvloeden. Deze virussen kunnen een aanhoudende lichte ontsteking veroorzaken, een aantasting van de epitheliale barrière, een wijziging van de microbiota en een verstoring van de werking van de schildklier en het enterische zenuwstelsel.
Deze aanhoudende ontsteking bevordert de ontregeling van de strakke verbindingentussen enterocyten, verhoogt de darmpermeabiliteit (“leaky gut”) en vergemakkelijkt de translocatie van bacteriële fragmenten of lipopolysacchariden in de bloedsomloop. Dit leidt tot een vicieuze cirkel: de aangetaste barrière zorgt voor meer contact tussen microbiële antigenen en het immuunsysteem, wat de ontsteking in stand houdt, de samenstelling van de microbiota negatief beïnvloedt en kan bijdragen aan functionele darmstoornissen, immuunonevenwichtigheden (toename van de prevalentie van auto-immuunziekten) en systemische manifestaties.
Adaptogene paddenstoelen die rijk zijn aan polysacchariden (β-glucanen) (Reishi, Cordyceps, Pruikzwam of Chaga) en astragaluswortel hebben verschillende biologische effecten die de spijsvertering, de motiliteit en de immuunregulatie kunnen ondersteunen in een SIBO-context die gepaard gaat met een chronische virale belasting.
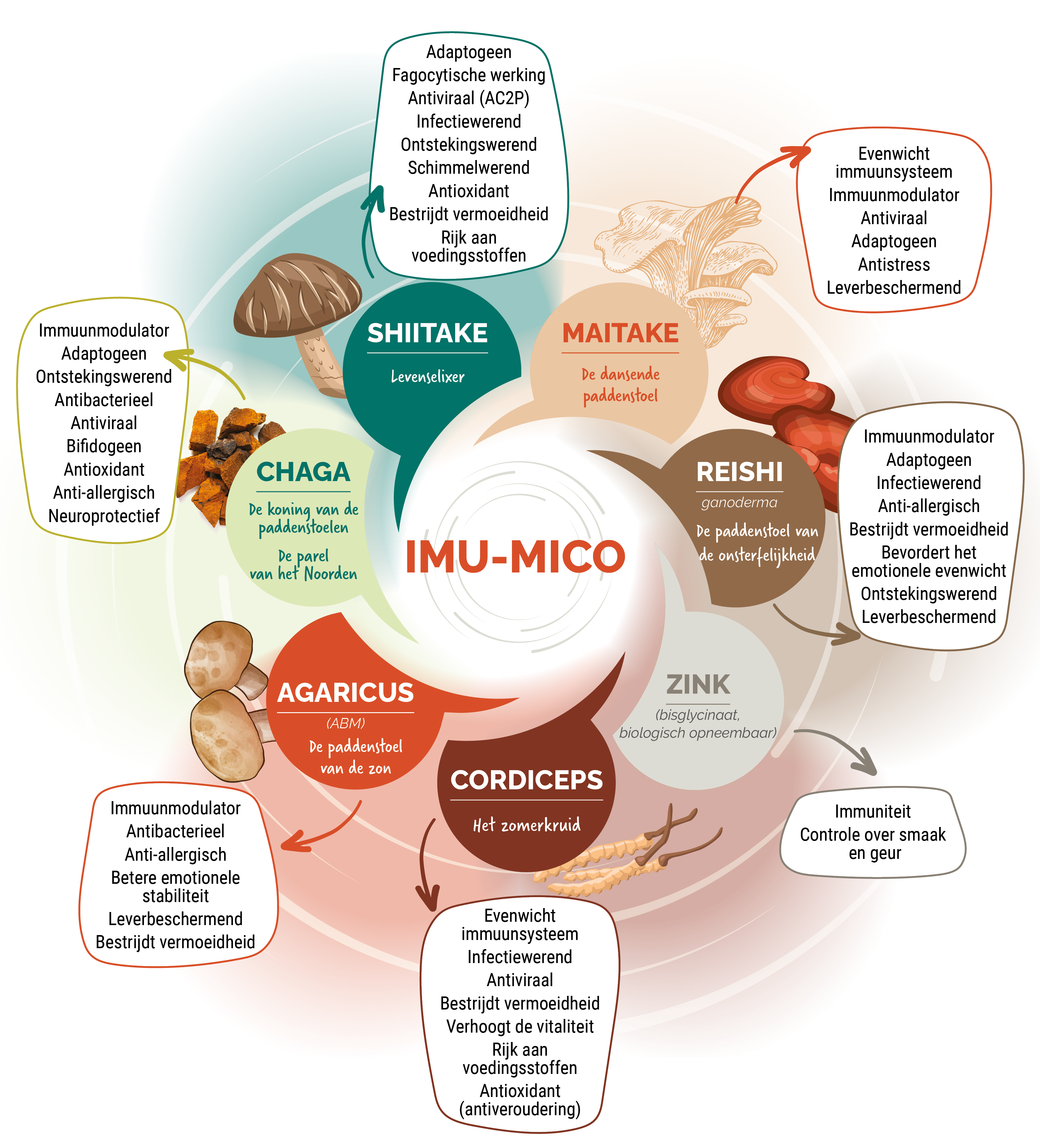
→ Ontdekken IMU-MICO
NATUURLIJKE BENADERINGEN BIJ DE BEHANDELING VAN SIBO
Het belang van mondgezondheid
Mondgezondheid gaat verder dan alleen tandhygiëne: het beïnvloedt de microbiële ecologie van het volledige spijsverteringskanaal. Studies hebben aangetoond dat bepaalde mondbacteriën, zoals Streptococcus, naar de darmen kunnen migreren en zich daar kunnen vestigen. Bij patiënten met inflammatoire darmziekten (IBD) zijn bijvoorbeeld identieke stammen aangetroffen in het speeksel en de ontlasting, wat duidt op ectopische kolonisatie (15).
Deze ‘mond-darm-as’ heeft fysiopathologische gevolgen: het binnendringen van mondbacteriën in de dunne darm kan een ongepaste bacteriële overgroei (SIBO) bevorderen, de slijmvliesbarrière aantasten en ontstekingen veroorzaken. Bij IBS-D-patiënten is de diversiteit van het tongmicrobiota verminderd, met een oververtegenwoordiging van Veillonella en Prevotella en een afname van Streptococcus, Haemophilus, Rothia en Granulicatella (16).
Op basis van deze gegevens wijzen de resultaten erop dat de mondflora actief kan bijdragen aan darmdysbiose. Slechte mondhygiëne, tongdysbiose of de overgroei van bepaalde orale soorten kunnen zo SIBO bevorderen of in stand houden. (17).
Low-FODMAP vs bifasisch
» welke strategie kiezen?
Bij de behandeling van SIBO is het belangrijk om duidelijk onderscheid te maken tussen het low-FODMAP-dieet en het bifasische dieet. Het low-FODMAP-dieet richt zich op het verminderen van spijsverteringssymptomen door het beperken van fermenteerbare koolhydraten, zonder rechtstreeks in te werken op de bacteriële overgroei. Het bifasisch dieet daarentegen, specifiek ontwikkeld voor SIBO, verloopt in twee fasen: een initiële, strikte fase die erop gericht is om de bacteriële flora in de dunne darm uit te hongeren door de fermenteerbare substraten sterk te beperken, gevolgd door een fase van geleidelijke herintroductie van goed verdragen voedingsmiddelen.
Deze methode zorgt niet alleen voor een snelle verlichting van de symptomen, maar vormt ook een strategie om het risico op terugval te verminderen en het microbiota opnieuw in balans te brengen. In tegenstelling tot het low-FODMAP-dieet, richt deze aanpak zich op de pathofysiologie van SIBO en biedt het een aanpak die verder gaat dan alleen symptomatische verlichting.
Zoom op bepaalde actieve stoffen
Colloïdaal zilver
» een waardevol hulpmiddel in een integratieve strategie.
Colloïdaal zilver, met name in de vorm van nanodeeltjes, wordt tegenwoordig erkend als een interessant mondantisepticum dat gericht kan inwerken op de gehele mondflora. Zilverionen hebben een veelzijdige antimicrobiële werking met een breed spectrum, waardoor ze bijzonder effectief zijn voor het reinigen van de mondholte.
Verschillende klinische studies hebben aangetoond dat mondspoelingen met zilvernanodeeltjes (AgNP’s) tandplak, de populaties van Streptococcus mutans – één van de belangrijkste bacteriën die betrokken zijn bij orale dysbiose – evenals de markers van tandvleesontsteking, doeltreffend verminderen. In sommige studies (18) blijkt hun doeltreffendheid vergelijkbaar met die van chloorhexidine, terwijl ze beter worden verdragen en geen tandverkleuring veroorzaken. Deze resultaten tonen aan dat colloïdaal zilver een modern, natuurlijk en doeltreffend alternatief vormt.
- Een doorslaggevende werking op de mondbiofilm, essentieel voor het voorkomen van herinfecties van het spijsverteringsstelsel.
Naast het simpelweg verminderen van vrije bacteriën, hebben zilvergebaseerde formuleringen nog een groot voordeel: ze zijn in staat de orale biofilm te desorganiseren. Deze biofilm – een echt microbiëel “reservoir” – speelt een centrale rol bij terugkerende recidieven van dysbiose in het spijsverteringsstelsel, waaronder bepaalde gevallen van SIBO waarbij de bron van besmetting de mondholte is. Door de cohesie van de biofilm te verminderen en de densiteit van pathogene bacteriën te verlagen, draagt colloïdaal zilver bij tot het beperken van herhaalde herkolonisatie van het spijsverteringskanaal, in het bijzonder in situaties waarin bacteriën van orale oorsprong migreren naar de dunne darm (19).
Hericium erinaceus
Hericium erinaceus is een paddenstoel die rijk is aan polysachariden en andere bioactieve verbindingen die het darmflora moduleren, ontstekingen verminderen en oxidatieve stress helpen beperken. Het heeft ontstekingsremmende effecten, waaronder de remming van NF-κB-signalering en regulering van cytokines. Hij staat bekend om zijn neuroprotectieve eigenschappen, die neuroregeneratie bevorderen.
Hericium ondersteunt de ontwikkeling van verschillende gunstige bacteriën, waaronder Bifidobacterium, Lactobacillus, Roseburia, Blautia, Anaerostipes, Sutterella en Desulfovibrio, terwijl het tegelijkertijd de overgroei van potentieel pathogene bacteriën vermindert (20).
Deze modulatie vermindert de productie van endotoxinen, met name LPS (lipopolysacchariden), en draagt zo bij tot een vermindering van systemische ontstekingen en microcirculatoire verstoringen. Deze mechanismen zijn vooral relevant bij SIBO, waarbij de darmpermeabiliteit en de disfunctie van het enterische zenuwstelsel (inclusief de nervus vagus) een rol kunnen spelen in de symptomatologie.
Antieke balsem uit Jeruzalem
De antieke balsem van Jeruzalem is een traditioneel elixer met een zeer oude oorsprong dat al eeuwenlang in het Midden-Oosten en Europa wordt gebruikt. De formule combineert mirre (guggul), wierook (boswellia), aloë vera, mastiek (Pistacia Lentiscus) en pepermunt, die samen een synergetische werking hebben op het hele spijsverteringskanaal. Het staat bekend om zijn ontstekingsremmende, antimicrobiële, antioxiderende en slijmvliesbeschermende eigenschappen.
Het wordt bijzonder aanbevolen om de maaglediging te vergemakkelijken en het maagslijmvlies te helpen herstellen, en als ontstekingsremmer van lage vetgraad waardoor het een waardevol middel is bij SIBO en functionele colopathie.
Butyraat
Butyraat is een korteketen vetzuur (SCFA) dat van nature in de dikke darm wordt geproduceerd door de fermentatie van voedingsvezels door de darmflora. Het speelt een sleutelrol in de spijsvertering en metabolisme. Het is een postbioticum, d.w.z. een bioactieve metaboliet die door darmbacteriën wordt geproduceerd en gunstige effecten uitoefent op de gastheer, ongeacht de aanwezigheid van levende bacteriën.
Butyraat wordt door de mitochondriën gemetaboliseerd als energiebron (ATP) voor de cellen van de dikke darm. Bij SIBO kunnen dysbiose en een tekort aan bacteriën die korteketenvetzuren (en dus butyraat) produceren, bijdragen aan een verhoogde slijmvliespermeabiliteit, lokale ontstekingen en een verminderde darmmotiliteit. Microbiotastudies tonen aan dat het niveau van SCFA’s (waaronder butyraat) bij een onevenwichtige voeding en darmdysbiose daalt.
Op klinisch vlak zijn micro-ingekapselde vormen van oraal butyraatgetest en melden verbeteringen van het maag-darmstelsel (opgeblazen gevoel, diarree/constipatie, buikpijn, misselijkheid, braken, winderigheid) en SIBO-markers.
Butyraat kan daarom overwogen worden als therapeutisch hulpmiddel bij SIBO om de epitheliale integriteit te ondersteunen, slijmvliesontsteking te verminderen en de darmmotiliteit te verbeteren.

Protocollen



Références bilbliographiques :
(1) Leite, G., Rezaie, A., Mathur, R., Barlow, G. , Rashid, M., Hosseini, A., Wang, J., Parodi, G., Villanueva‑Millán, M. J., Sanchez, M., Morales, W., Weitsman, S., & Pimentel, M. (2024). Defining Small Intestinal Bacterial Overgrowth by Culture and High Throughput Sequencing. Clinical Gastroenterology and Hepatology, 22(2), 259‑270.
(2) Li, J., Wang, J., Zhang, R., et al. (2021). Mucosa-Associated Microbial Profile Is Altered in Small Intestinal Bacterial Overgrowth. Frontiers in Microbiology, 12, 710940.
(3) Jacob T Barlow et al. Quantitative sequencing clarifies the role of disruptor taxa, oral microbiota, and strict anaerobes in the human small-intestine microbiome. 2021 Nov 2; 9:214.
(4) Taojun Wang et al. In vitro interactions between Blautia hydrogenotrophica, Desulfovibrio piger and Methanobrevibacter smithii under hydrogenotrophic conditions. Gut Microbes. 2023 Sep 27;15(2):2261784.
(5) Christian Boyer, Mai 2024, Le SIBO ou pullulation bactérienne de l’intestin grêle, blog de Dyjest, https://blog.dyjest.care/posts/sibo-part-1/
(6) Mark Pimentel et al. Lower Frequency of MMC Is Found in IBS Subjects with Abnormal Lactulose Breath Test, Suggesting Bacterial Overgrowth. Digestive Diseases and Sciences, Vol. 47, No. 12 (2002), pp. 2639–2643.
(7) Mehrnaz Nikkhah Bodaghet al.(2018). Ginger in gastrointestinal disorders: A systematic review of clinical trials. Food Sci Nutr. 2018 Nov 5;7(1):96–108.
(8) Andrew C. Dukowicz et al. (2007). Small Intestinal Bacterial Overgrowth: A Comprehensive Review. Gastroenterology & Hepatology Volume 3, Issue 2.
(9) Tingting Su et al. (2017). Meta-analysis: proton pump inhibitors moderately increase the risk of small intestinal bacterial overgrowth. J Gastroenterol. 2018 Jan;53(1):27-36.
(10) Alsu R Khurmatullina (2025). The Duration of Proton Pump Inhibitor Therapy and the Risk of Small Intestinal Bacterial Overgrowth: A Systematic Review and Meta-Analysis. J Clin Med. 2025 Jul 3;14(13):4702.
(11) Xu, G.-M., Hu, M.-X., Li, S.-Y., Ran, X., Zhang, H., & Ding, X.-F. (2024). Thyroid disorders and gastrointestinal dysmotility: An old association. Frontiers in Physiology, 15, Article 1389113.
(12) Ceylan Tanes et al. (2021). Gut Microbiome Changes Associated with Epithelial Barrier Damage and Systemic Inflammation during Antiretroviral Therapy of Chronic SIV Infection. 2021 Aug 8;13(8):1567.
(13) Antonella Gallo et al. (2025). Intestinal Inflammation and Permeability in Patients Recovered from SARS-CoV-2 Infection. Dig Dis. 2025;43(1):1-10.
(14) Zachary J. Morse et al. (2021). Virus Infection Is an Instigator of Intestinal Dysbiosis Leading to Type 1 Diabetes. Immunol., Sec. Immunological Tolerance and Regulation, Volume 12.
(15) Kitamoto, S., Nagao-Kitamoto, H., Hein, R., Schmidt, T. M., & Kamada, N. (2020). The Bacterial Connection between the Oral Cavity and the Gut Diseases. Journal of Dental Research, 99(9), 1021-1029.
(16) Li, Y., Mai, Y., Jiao, Y., Yuan, Y., Qu, Y., Zhang, Y., Wang, M., Zhang, W., Lu, X., Lin, Z., Li, J., Mao, T., & Xie, C. (2025, février). Alterations in the tongue coating microbiome in patients with diarrhea-predominant irritable bowel syndrome: A cross-sectional study. APMIS, 133(2), e70001.
(7) Abdelbary, M. M. H., Hommola, A. K., Diederichs, A., Knueppel, L., Bode, A., Depner, M., … & Ott, S. (2022). The oral-gut axis: Salivary and fecal microbiome dysbiosis in inflammatory bowel disease. Frontiers in Cellular and Infection Microbiology, 12, Article 1010853.
(18) Thao, D. T., Nguyen Thi, Y. H., Le Nguyen, D. H., Dang The, A. T., Tru Nguyen, C. P., Nguyen, V. T., Quach, U. N., & Truong, L. T. (2025). Comparing the Effectiveness of 0.12% Chlorhexidine and Silver Nanoparticles Mouthwashes: A Double-Blind Randomized Controlled Trial Among Medical Students in Southern Vietnam. Cureus, 17(7), e87948.
(19) Raghav, P., Khera, A. , & Bisht, S. (2025). Comparative evaluation of antimicrobial properties of silver nanoparticles and chlorhexidine mouthwashes on the colonization of microflora and oral health during orthodontic treatment: A double‑blind randomized controlled trial. Dental Press Journal of Orthodontics, 30(1), e2524112.
(20) Miaoyu Li et al. (2021). Role of dietary edible mushrooms in the modulation of gut microbiota. Journal of Functional Foods 83 (2021) 104538.
(21) George B. Saffouri et al. (2019) Small intestinal microbial dysbiosis underlies symptoms associated with functional gastrointestinal disorders. Nature communications (2019) 10:2012.
Document réservé à l’usage des praticiens de santé.
