
INTRODUCTION
La douleur chronique est une condition complexe et souvent incomprise, marquée par une grande diversité de manifestations, qui varient largement d’un individu à l’autre. On parle de douleur chronique lorsqu’une douleur persiste au-delà de trois mois, dépassant la durée normale de guérison.
Elle peut être liée à une pathologie identifiée – comme une neuropathie, une inflammation ou un cancer – mais elle persiste parfois sans cause organique évidente.
D’origine multidimensionnelle, la douleur chronique résulte de mécanismes physiopathologiques complexes, souvent entrelacés avec des facteurs psychologiques et sociaux. Cette complexité contribue non seulement à la difficulté du diagnostic, mais aussi à celle de la prise en charge, qui nécessite une approche globale, individualisée et souvent pluridisciplinaire, centrée sur la réalité vécue par chaque patient.
Souvent, les personnes concernées traversent une errance thérapeutique, d’autant plus que certains types de douleurs chroniques imitent ou se confondent avec d’autres troubles, rendant leur reconnaissance et leur traitement plus ardus. Cette réalité en fait aujourd’hui un véritable enjeu de santé publique.
Afin d’éclairer ce phénomène encore trop peu compris dans toute sa richesse et sa complexité, parcourons ensemble les dernières avancées scientifiques sur le sujet, pour mieux comprendre les types de douleurs chroniques, leurs causes multifactorielles, et les protocoles naturels et intégratifs qui permettent une prise en charge plus efficace.
Les types de douleurs
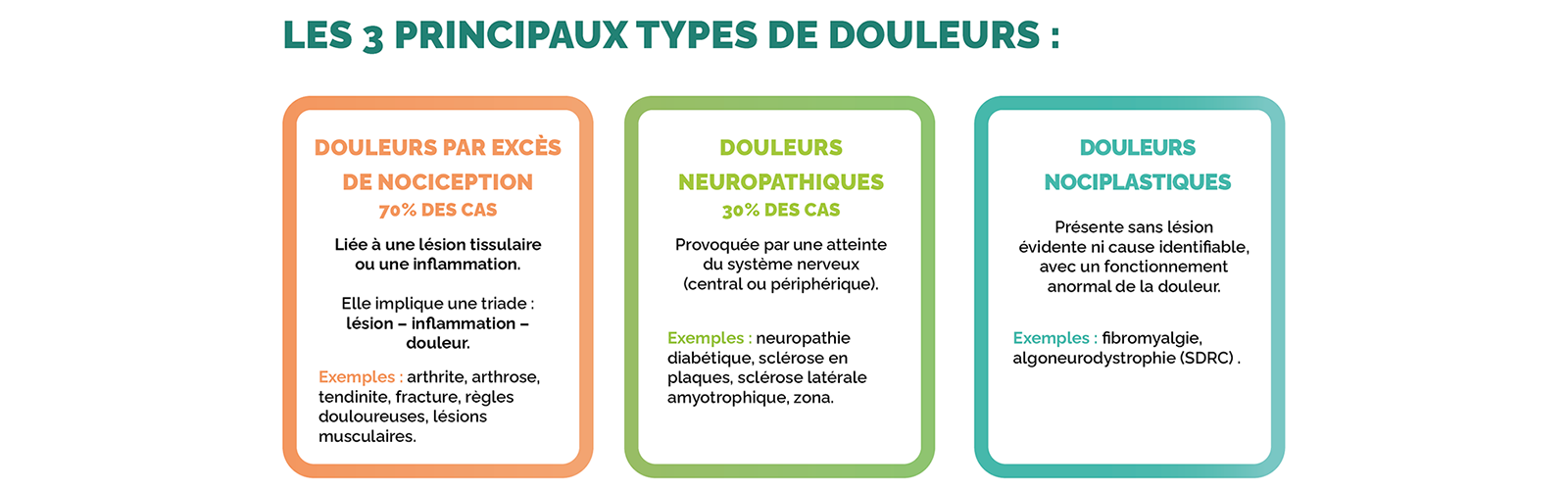

Les différentes causes multifactorielles
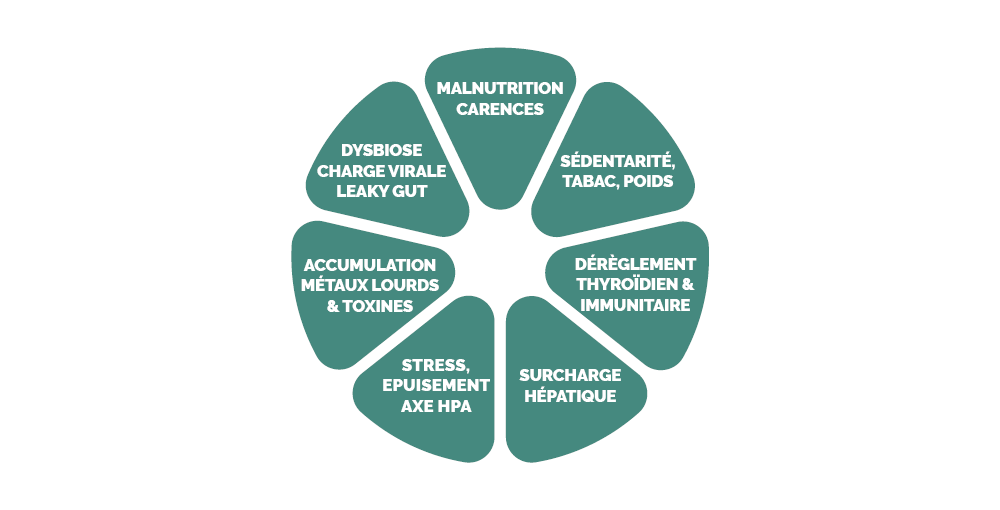
La douleur chronique est une problématique complexe, dont les origines et facteurs aggravants sont souvent multiples et intriquées. Elle ne peut se résumer à une simple lésion ou à un déséquilibre isolé, mais résulte plutôt d’un ensemble de facteurs biologiques, psychologiques et environnementaux qui interagissent entre eux.
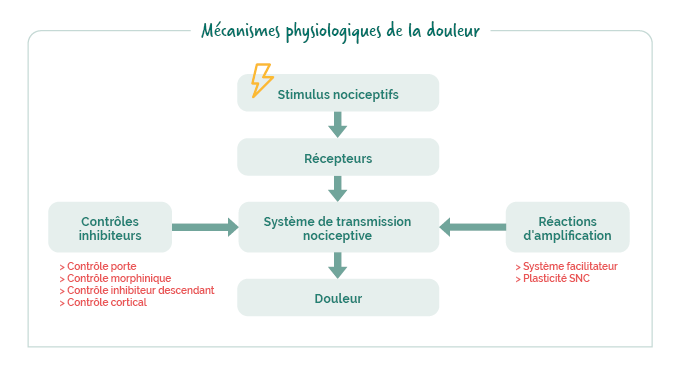
Les mécanismes physiologiques de la douleur
La douleur débute par un stimulus nociceptif (lésion tissulaire, inflammation, distension, etc.) capté par des nocicepteurs périphériques, qui sont des terminaisons nerveuses libres exprimant des canaux ioniques spécifiques sensibles aux stimuli mécaniques, thermiques ou chimiques.
L’activation de ces récepteurs engendre un potentiel d’action qui est transmis par les fibres afférentes (A-delta et C) jusqu’à la corne dorsale de la moelle épinière. Le signal est ensuite intégré et relayé via le système de transmission nociceptive, qui intègre les voies nerveuses allant de la périphérie jusqu’au cerveau. C’est à ce stade que la douleur est perçue.
DOULEURS CHRONIQUES ET INFLAMMATION
Les facteurs favorisants
Inflammation de bas grade et neuro-inflammation
L’inflammation chronique de bas grade, se caractérise par une activation prolongée mais modérée du système immunitaire inné, sans les signes cliniques classiques de l’inflammation aiguë (chaleur, rougeur, œdème). Elle est le reflet d’un état d’alarme corporel élevé qui passe souvent inaperçu ou qui n’est pas écouté. Cet état joue un rôle central dans de nombreuses maladies responsables de douleurs chroniques. Les cellules immunitaires libèrent des médiateurs inflammatoires qui sensibilisent les neurones périphériques et centraux, perturbant la transmission de la douleur. Elles peuvent aussi infiltrer la moelle épinière et les ganglions dorsaux. Cette activation inflammatoire prolongée influence également l’humeur, le comportement et serait impliquée dans plusieurs troubles psychiatriques : troubles de l’humeur, addictions, schizophrénie, TDAH, autisme (1).
En outre, il est important de noter que le tabagisme, la consommation d’alcool, l’obésité, les antécédents de douleur chronique et les facteurs psychologiques (comme le stress et l’anxiété) sont tous des facteurs à ne pas négliger, qui entretiennent ce phénomène inflammatoire.
Dysbiose intestinale, fonction hépatique et douleurs chroniques
La dysbiose intestinale, caractérisée par une perturbation de l’équilibre du microbiote, favorise une augmentation de la perméabilité intestinale (« leaky gut ») permettant la translocation dans la circulation systémique de lipopolysaccharides (LPS) et autres toxines microbiennes (2). Ces composés liposolubles nécessitent une transformation hépatique via les phases I et II de détoxification afin d’être convertis en molécules hydrosolubles éliminables. Lorsque cette capacité est dépassée, il en résulte une accumulation toxique systémique, affectant particulièrement les tissus riches en lipides comme le cerveau (composé d’environ 60 % de lipides), favorisant ainsi la neurotoxémie (3).
Rôle central du foie dans la modulation de la douleur
La dysbiose intestinale et la surcharge hépatique induisent une activation persistante du système immunitaire, libérant des cytokines pro-inflammatoires (TNF-α, IL-6, IL-1β) qui traversent la barrière hémato-encéphalique et activent la microglie cérébrale (4). Ce phénomène est au cœur des mécanismes de neuro-inflammation chronique responsables de la sensibilisation centrale à la douleur, un processus clé dans les douleurs neuropathiques et chroniques (5).
Le foie, en neutralisant ces toxines liposolubles, joue un rôle clé dans la prévention de la neurotoxémie. Le soutien des phases de détoxification hépatique, particulièrement la phase II (conjugaison), est crucial pour réduire la charge toxique systémique et l’inflammation périphérique qui entretiennent la douleur neuropathique (6).
Les déficits en glutathion, principal antioxydant cellulaire et cofacteur majeur de la phase II, amplifient l’impact neurotoxique en réduisant la capacité de neutralisation des radicaux libres et métabolites toxiques (7).
- Sur le schéma, nous pouvons observer les différentes phases de détoxification hépatique et les micronutriments favorisant l’activation de ces différentes phases.
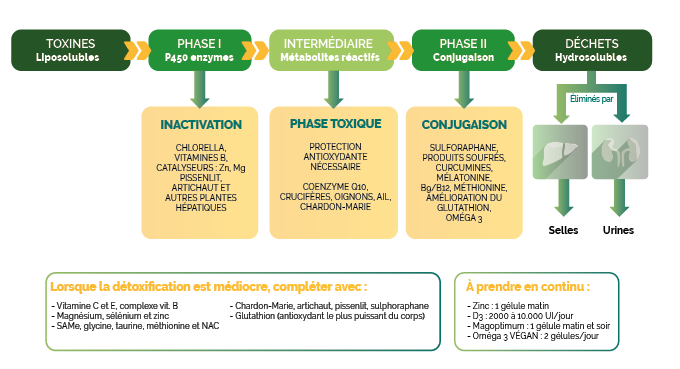
En renforçant la détoxification hépatique, ces micronutriments contribuent à réduire la neuro-inflammation et la sensibilisation centrale, offrant un axe thérapeutique pertinent dans la prise en charge des douleurs neuropathiques chroniques.
Stress et épuisement de l’axe HPA
Le stress prolongé induit une activation persistante de l’axe hypothalamo-hypophyso-surrénalien (HPA), avec hyperproduction de cortisol, puis un épuisement progressif du système, résultant en une réponse dysrégulée de l’axe HPA (8). Cette dysrégulation contribue à une sensibilisation des circuits de la douleur et favorise le passage à une douleur chronique.
À long terme, des taux élevés de cortisol (9) perturbent la plasticité synaptique, en particulier au niveau du cortex préfrontal et de l’hippocampe. Ces altérations favorisent une hyperexcitabilité de la corne dorsale de la moelle épinière et une centralisation de la douleur, rendant les systèmes de perception plus réactifs aux stimuli, même faibles. En parallèle, le stress stimule la libération de cytokines pro-inflammatoires, telles que l’IL-6 et le TNF-α, qui peuvent franchir la barrière hémato-encéphalique (10). Ces cytokines activent les cellules microgliales du système nerveux central, entretenant un état de neuro-inflammation persistante (11).
Cette activation microgliale prolongée influence la transmission des signaux nociceptifs, contribuant à maintenir un état de vigilance douloureuse accrue.
Par ailleurs, le stress chronique altère le métabolisme du tryptophane en augmentant l’activité de l’enzyme IDO (indoleamine-2,3-dioxygénase), détournant ainsi le tryptophane de la voie sérotoninergique vers la production de kynurénines neuroactives. Ces métabolites peuvent activer les récepteurs NMDA (N-Méthyl-D-Aspartate), renforçant l’excitation neuronale et l’excitotoxicité, aggravant ainsi la douleur perçue (12)(13).
Les répercussions cliniques incluent : troubles du sommeil, fatigue chronique, céphalées, hypersensibilité au stress, déclin cognitif, fréquents dans les pathologies telles que la fibromyalgie, la neuropathie (14).
Il s’installe alors un cercle vicieux dans lequel le stress et la douleur s’auto-alimentent : le stress favorise l’inflammation et la douleur, tandis que la douleur chronique renforce la perception du stress, via les mêmes voies neuroendocriniennes et immunitaires. Cette interaction bidirectionnelle entre douleur et inflammation rend la sortie du processus d’autant plus complexe sans une approche globale et multidisciplinaire.

Une interaction bidirectionnelle établie
L’inflammation de bas grade agit comme un terrain propice à lachronicisation de la douleur, en entretenant une sensibilisation des voies nociceptives centrales et périphériques.
Des recherches cliniques et expérimentales ont démontré que :
- Chez les patients présentant des douleurs musculosquelettiques chroniques, des taux circulants accrus de cytokines pro-inflammatoires, en particulier l’IL-6 et le TNF-α, ont été corrélés à l’intensité perçue de la douleur (15).
- Dans la fibromyalgie — considérée comme un prototype de douleur nociplastique — une méta-analyse a révélé des élévations significatives de certains médiateurs inflammatoires, suggérant que même en l’absence de dommage tissulaire identifiable, une inflammation de bas grade peut influencer la symptomatologie douloureuse (16).
- Des études de neuroimagerie ont objectivé l’activation de la microglie cérébrale dans un contexte d’inflammation périphérique chronique. Cette activation gliale contribue à la neuro-inflammation et à la sensibilisation centrale, des mécanismes clés dans la transition vers une douleur chronique (17).
- Sur le plan neuro-immunologique, des cytokines telles que l’IL-1β et le TNF-α ont été impliquées dans l’altération de la conduction nerveuse et l’augmentation de l’excitabilité des fibres nociceptives, notamment après une lésion nerveuse (18).
- Enfin, une dérégulation du métabolisme du tryptophane, sous l’effet d’une activation excessive de NF-κB en contexte inflammatoire, peut entraîner une shunt vers la voie du kynurénine au détriment de la synthèse de sérotonine. Certains métabolites issus de cette voie, comme la quinolinique, activent le récepteur NMDA (N-Méthyl-D-Aspartate), amplifiant ainsi les phénomènes d’hyperalgésie et de sensibilisation (19). Cette dérivation métabolique rend l’usage du tryptophane délicat dans certaines douleurs nociplastiques car il risquerait de devenir hyperalgique, en particulier si l’inflammation n’est pas maîtrisée.
Les marqueurs clés du terrain inflammatoire
À ce jour, il n’existe pas de biomarqueur unique permettant de diagnostiquer formellement une inflammation chronique de bas grade. Toutefois, plusieurs paramètres biologiques, interprétés conjointement avec l’anamnèse et le tableau clinique, permettent de renforcer la suspicion d’un terrain inflammatoire silencieux. Ces marqueurs reflètent une activation persistante du système immunitaire inné et une désorganisation des régulations métaboliques et
neuro-immunes.
1. CRP Ultrasensible (CRPus)
Contrairement à la CRP standard, la CRP ultrasensible permet de détecter des élévations faibles (0,3 à 10 mg/L), typiques de l’inflammation silencieuse (20).
- < 1 mg/L : risque faible (inflammation minime)
- 1–3 mg/L : inflammation modérée
- 3 mg/L : inflammation significative de bas grade
2. Électrophorèse des protéines plasmatiques (EPP)
Permet de rechercher des modifications subtiles dans les fractions protéiques (21).
- ↗︎ Alpha-1-globulines (ex : α1-antitrypsine, orosomucoïde) : caractérise la phase inflammatoire aiguë.
- ↗︎ Alpha-2-globulines (haptoglobine, α2-macroglobuline) et ↘︎ Albumine : caractérise une inflammation chronique.
3. Statut en acides gras (rapport oméga-6/oméga-3)
Un déséquilibre du rapport AA/EPA (AA : acide arachidonique) ou Oméga-6/Oméga-3 (>10) est souvent associé à un terrain inflammatoire chronique. Un rapport > 10 est associé à une activation pro-inflammatoire du métabolisme lipidique et à une stimulation des voies dérivées de l’acide arachidonique (PGE2, LTB4…) (22).
4. Ferritine sérique
Lorsque la ferritine est modérément élevée avec une saturation en fer normale ou basse, elle peut traduire un état inflammatoire chronique (hors hémochromatose) (23).
Évolution des différents paramètres biologiques au cours d’une anémie ferriprive à caractère inflammatoire :
- Hémoglobine – En baisse ↘︎
- Fer – En baisse ↘︎
- Taux de saturation – Normal ou basse ↘︎
- Ferritine – Normal ou haute ↗︎
Source : https://www.revmed.ch/revue-medicale-suisse/2011/revue-medicale-suisse-313/anemie-ferriprive-inflammatoire-ou-mixte-comment-orienter-le-diagnostic
5. Homocystéine
L’augmentation de l’homocystéine est associée à un risque cardiovasculaire mais aussi à une activation de la microglie et à des douleurs neuropathiques selon certaines études. Il est aussi important de vérifier le dosage en B12 active et B9 érythrocytaire lorsqu’on dose l’homocystéine car une homocystéine élevée peut-être en lien avec une carence en B12 et B9 (24).
6. Zonuline
La zonuline, régulatrice des jonctions serrées intestinales, est un marqueur indirect de la perméabilité intestinale. Son élévation favorise le passage de LPS et de fragments bactériens dans la circulation systémique, stimulant le TLR4 (Toll-Like Receptor 4) (25).
7. LPS (Lipopolysaccharides) et LBP (LPS-binding protein)
- Le LPS est un composant des bactéries Gram−, son passage dans la circulation stimule TLR4 et par conséquent, la cascade inflammatoire (26).
- LBP est une protéine du foie qui se lie au LPS : sa concentration augmente avec la charge de LPS circulant (27).

- CRP Ultrasensible (CRPus)
- Électrophorèse des protéines plasmatiques (EPP)
- Statut en acides gras
- Ferritine sérique
- Homocystéine
- Zonuline
- LPS et LBP
QUELLES SOLUTIONS ENVISAGER
Le potentiel du PEA
Le PEA est un lipide endogène naturel, produit instantanément et localement par l’organisme en réponse à certaines stimulations du corps : inflammation, infection, intoxication, blessure, traumatisme, et stress. Les scientifiques ont observé qu’il était produit en masse dans les tissus présentant une dégénération ou des lésions, donc en cas d’inflammation.
Le PEA constitue une forme de protection des tissus afin d’aider la réparation tissulaire. Il a un effet endocannabinoïde-like mais pas psychotrope afin de contrôler la perception de la douleur. Le PEA pourrait également être impliqué dans la désensibilisation des récepteurs à la chaleur, hyperactivés en cas d’inflammation.
Ce lipide endogène, analgésique et anti-inflammatoire, est particulièrement utile dans les douleurs neuropathiques par modulation de la microglie et activation du PPAR-α (Peroxisome Proliferator-Activated Receptor alpha).
Une revue systématique et méta-analyse, réalisée en 2023, a évalué l’efficacité du PEA dans le traitement de la douleur chronique. Sur les 253 articles identifiés, 11 études randomisées en double aveugle ont été incluses, totalisant 774 patients. Les résultats montrent que le PEA réduit significativement les scores de douleur par rapport au placebo ou à d’autres traitements. Des améliorations de la qualité de vie et de lafonction motrice ont également été rapportées, sans effets indésirables et interactions médicamenteuses majeurs (28).
Une autre étude randomisée en double aveugle contrôlée par placebo a évalué les mécanismes d’action du PEA chez 14 volontaires sains. Après 4 semaines de prise de PEA (3 × 400 mg/jour), plusieurs marqueurs de la douleur ont été mesurés. Les résultats montrent une diminution significative de la douleur induite, une amélioration de la tolérance au froid et à la pression, ainsi qu’une modulation favorable de la douleur (réduction de l’allodynie). Ces données suggèrent que la PEA exerce des effets analgésiques cliniquement pertinents via des mécanismes à la fois périphériques, centraux et modulatoires, notamment dans le cadre des douleurs nociplastiques (29).
Le potentiel du Gingembre
Le gingembre contient plus de 400 composés naturels, parmi lesquels les gingérols, shogaols et paradols sont les plus étudiés pour leurs effets anti-inflammatoires et antalgiques.
Le 6-gingérol, en particulier, est le principe actif dominant du gingembre frais, tandis que les shogaols, formés lors du séchage, sont plus puissants en termes d’effets thérapeutiques.
Ces molécules exercent une action modulatrice sur plusieurs voies de l’inflammation, en inhibant notamment la production de prostaglandines et de cytokines pro-inflammatoires (TNF-α, IL-1β, IL-6), des médiateurs clés dans les douleurs chroniques et la neuro-inflammation.

Mécanismes d’action impliqués dans la modulation de la douleur :
Le gingembre agit comme un inhibiteur non sélectif des voies cyclo-oxygénase (COX-1 et COX-2) et lipoxygénase (5-LOX), réduisant ainsi la production de prostaglandines (PGE2) et leucotriènes impliqués dans l’inflammation et la nociception (30). Cette action est comparable à celle de certains AINS, mais avec une meilleure tolérancegastro-intestinale.
De plus, les gingérols inhibent la translocation nucléaire de NF‑κB (facteur nucléaire kappa B des lymphocytes B activés), un facteur clé de l’activation des gènes pro-inflammatoires, entraînant une diminution de la production de TNF-α, IL‑1β et IL‑6. Cette action contribue à réduire la neuro-inflammation impliquée dans la chronicisation de la douleur (31).
Les composés phénoliques du gingembre sont capables de franchir la barrière
hémato-encéphalique et d’interagir avec les cellules immunitaires du cerveau, en particulier la microglie. Des études précliniques suggèrent que le gingembre favorise un phénotype
anti-inflammatoire (M2) des cellules microgliales, contribuant ainsi à un effet neuroprotecteur (32).
Son action antalgique s’explique par une inhibition de l’enzyme COX-2 (Cyclo-Oxygénase-2), impliquée dans l’inflammation, mais aussi par un effet régulateur sur les récepteurs de la douleur TRPV1 (Transient Receptor Potential Vanilloid 1) souvent suractivés en cas d’inflammation chronique. Ce sont ces mêmes récepteurs qui sont ciblés par la capsaïcine, utilisée pour réduire la transmission des signaux douloureux au niveau périphérique (33).
Pour finir, le gingembre réduit le stress oxydatif en augmentant l’activité des enzymes antioxydantes SOD (SuperOxyde Dismutase) et GPx (Glutathione Peroxydase), protégeant ainsi les neurones et tissus périphériques contre les dommages induits par les radicaux libres, fréquents en cas d’inflammation chronique (34).
Le potentiel du Krill
L’huile de krill se distingue par sa composition unique en acides gras oméga-3 (EPA et DHA)liés à des phospholipides, contrairement à l’huile de poisson où ils sont majoritairement sous forme de triglycérides. Cette forme phospholipidique améliore la biodisponibilité cellulaire, en particulier au niveau des membranes neuronales et immunitaires, ce qui est d’un intérêt majeur dans les douleurs chroniques d’origine inflammatoire ou neuropathique. Le krill contient également de l’astaxanthine, un puissant antioxydant aux effets neuroprotecteurs.
Les propriétés antalgiques et anti-inflammatoires du krill reposent sur plusieurs mécanismes complémentaires. Il diminue la production de cytokines pro-inflammatoires telles que le TNF-α et l’IL-6, impliquées dans la genèse et la pérennisation de la douleur chronique. Cette modulation permet de limiter la sensibilisation des nocicepteurs et l’excitabilité neuronale excessive.
Au niveau central, les oméga-3 du krill exercent une action inhibitrice sur l’activation excessive de la microglie, réduisant ainsi la neuro-inflammation et les phénomènes de sensibilisation centrale. En parallèle, le krill soutient le métabolisme énergétique neuronal par une amélioration de la fonction mitochondriale, contribuant à réduire la fatigue et la transmission douloureuse persistante. L’astaxanthine intervient en synergie, limitant la peroxydation lipidique et protégeant les membranes neuronales.

Des études récentes confirment que les oméga-3 marins, notamment ceux du krill, modulent favorablement les voies inflammatoires et oxydatives associées aux douleurs persistantes. En agissant simultanément sur les médiateurs périphériques et centraux, le krill s’impose comme une option naturelle prometteuse dans une approche intégrative de la douleur chronique (35).
Le potentiel de la Phycocyanine
La phycocyanine est un pigment protéique bleu naturellement présent dans les cyanobactéries comme la spiruline. Elle est dotée de puissantes propriétés antioxydantes, anti-inflammatoires et immunomodulatrices. Son profil bioactif unique, notamment par sa structure tétramérique riche en chromophores, lui permet d’interagir efficacement avec les radicaux libres et les médiateurs de l’inflammation.
Dans le cadre des douleurs chroniques, elle agit en inhibant la voie de signalisation NF-κB, entraînant une réduction de l’expression des cytokines pro-inflammatoires telles que l’IL-1β, l’IL-6 et le TNF-α. Elle module également l’activité de la COX-2 (Cyclo-Oxygénase-2), limitant ainsi la production de prostaglandines algogènes, sans les effets gastro-intestinaux indésirables associés aux anti-inflammatoires conventionnels.
Sur le plan neuroprotecteur, la phycocyanine réduit le stress oxydatif en inhibant la peroxydation lipidique, préservant ainsi l’intégrité des membranes neuronales, ce qui est particulièrement pertinent dans les douleurs d’origine neuropathique. Par ailleurs, des modèles précliniques suggèrent qu’elle potentialise les voies antinociceptives endogènes, notamment via l’activation des systèmes GABAergiques et opioïdes, renforçant son action analgésique centrale.

Des études expérimentales ont montré que la phycocyanine exerce des effets antalgiques comparables à ceux du paracétamol ou des AINS (anti-Inflammatoires Non Stéroïdiens), mais avec un excellent profil de tolérance, sans effets hépatiques ni digestifs notables (36, 37).
Le potentiel du Safran
Le safran, riche en composés bioactifs comme la crocine, le safranal et la picrocrocine, possède des propriétés analgésiques, anti-inflammatoires et neuromodulatrices bien documentées. Ces molécules agissent à la croisée des voies neuro-inflammatoires et neurotransmissionnelles, ce qui le rend particulièrement pertinent dans les douleurs chroniques d’origine mixte (nociceptive, neuropathique, nociplastique).
Sur le plan inflammatoire, le safran module la voie de signalisation NF-κB, entraînant une inhibition de la production de cytokines pro-inflammatoires telles que l’IL-6 et le TNF-α, impliquées dans la sensibilisation périphérique et centrale. Il exerce également une activité antioxydante cérébrale, limitant le stress oxydatif neuronal, un facteur majeur dans la genèse des douleurs chroniques centralisées.
Par ailleurs, le safran agit sur les systèmes sérotoninergique, dopaminergique et opioïde, contribuant à une élévation des seuils de douleur et à une amélioration de la tolérance nociceptive. Son action sur la neurotransmission est également corrélée à des effets positifs sur l’humeur, fréquemment altérée dans les syndromes douloureux chroniques. Cette modulation passe notamment par une régulation de la voie du tryptophane et une inhibition de la monoamine oxydase (MAO), renforçant son effet antidépresseur.
Des essais cliniques ont confirmé l’efficacité du safran dans la réduction de la douleur dans plusieurs affections chroniques telles que la dysménorrhée, la fibromyalgie ou les lombalgies, ainsi qu’en tant que soutien complémentaire dans les états dépressifs (38, 39).

APPROCHE NATURELLE
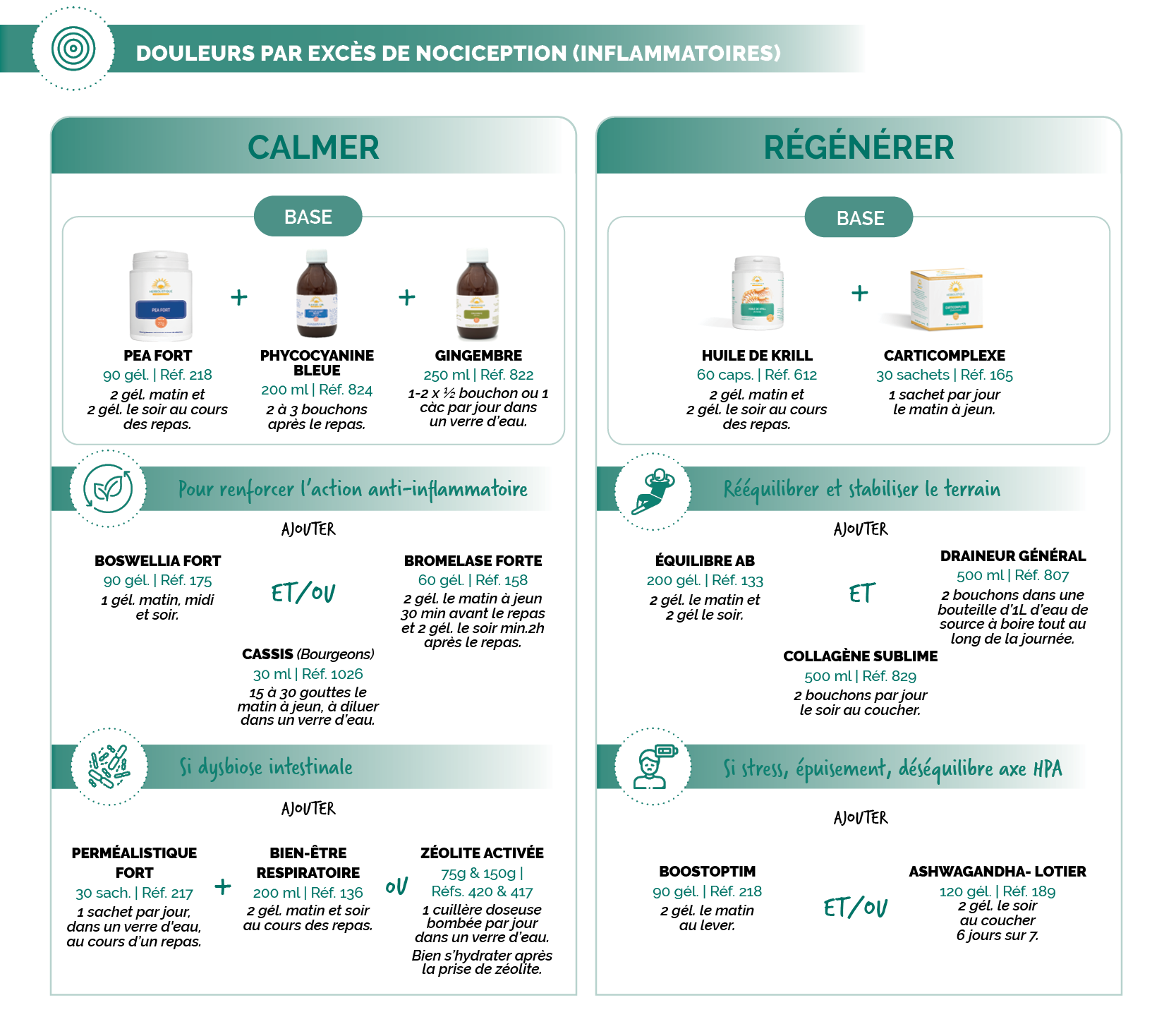
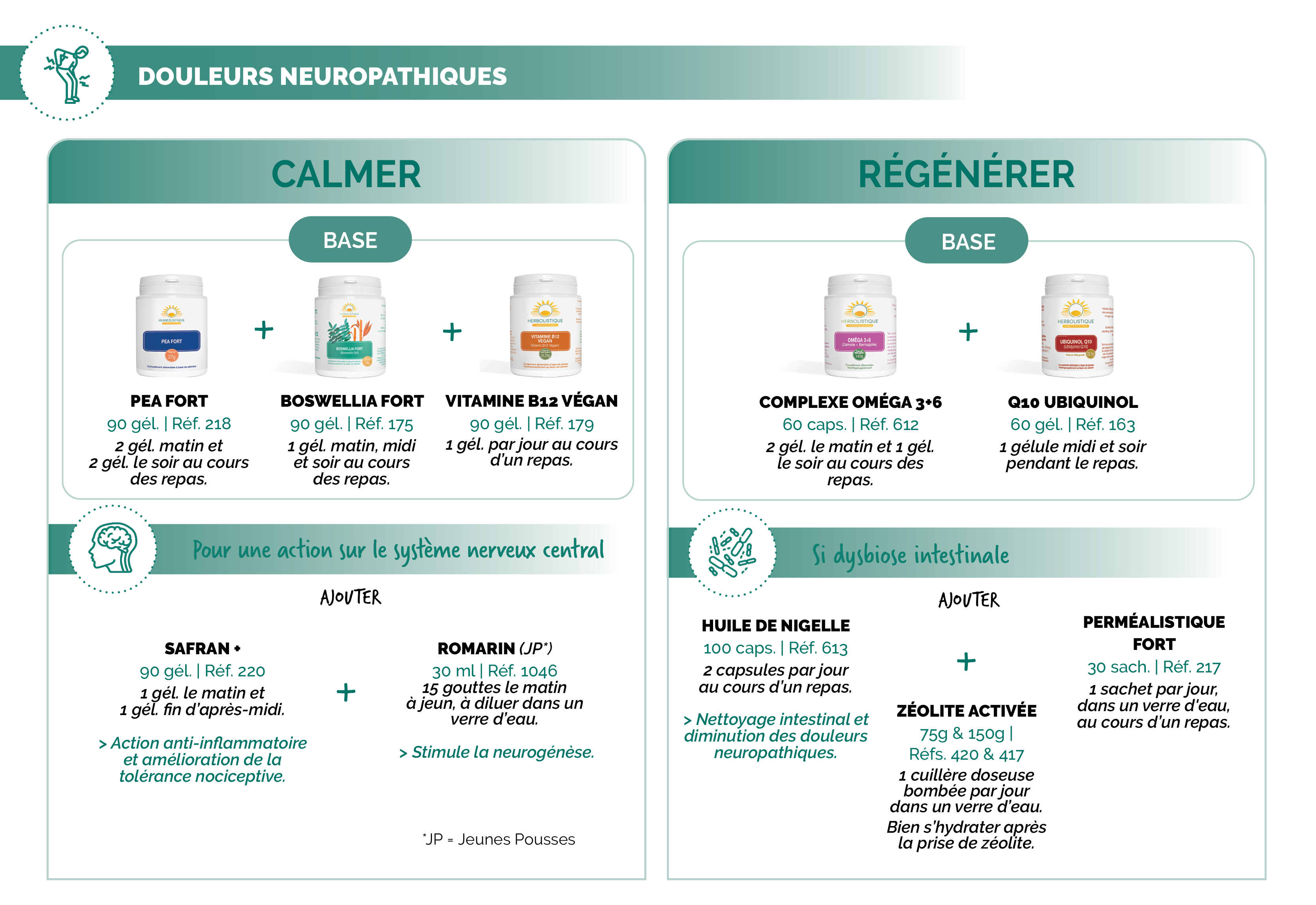
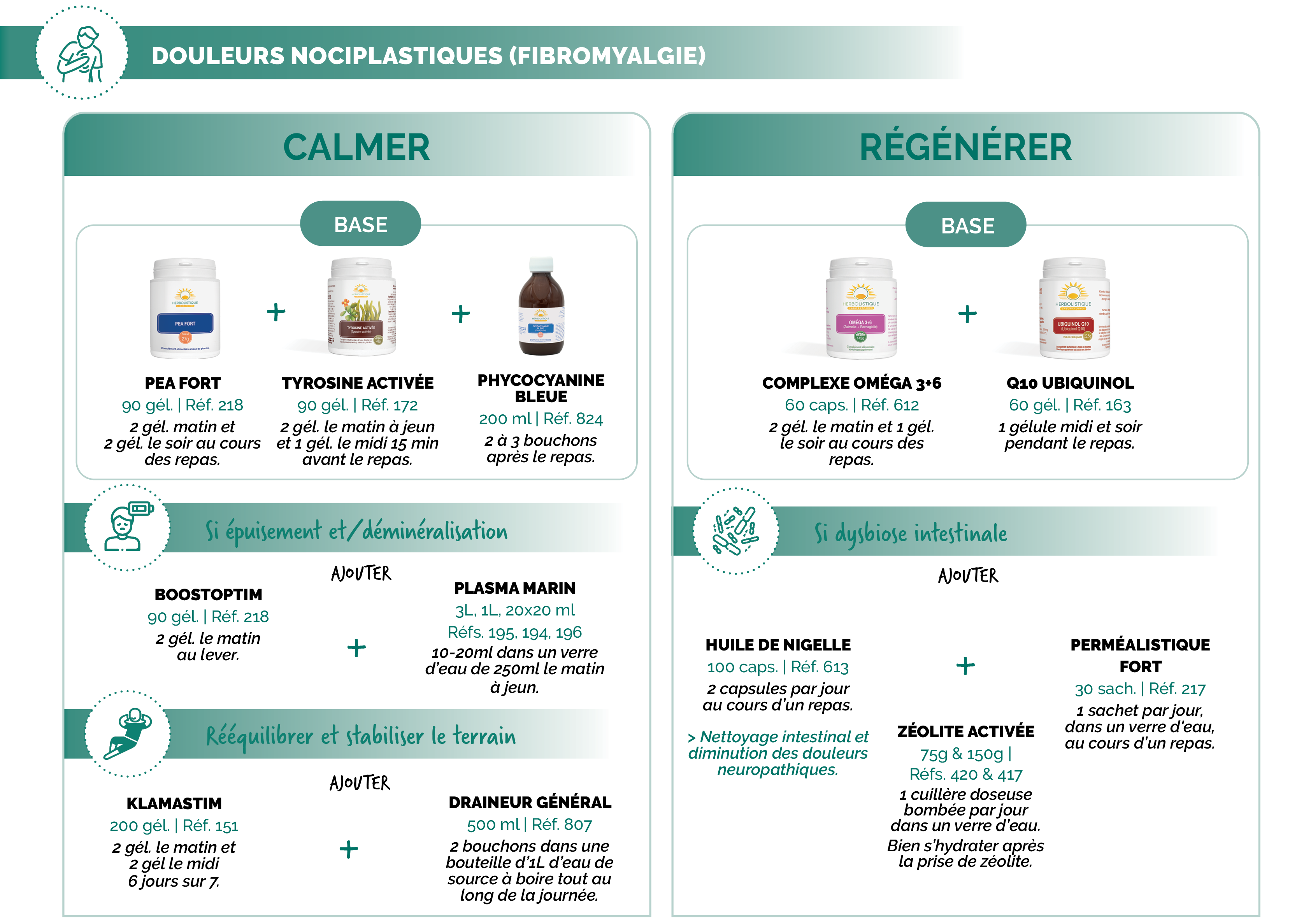
Suggestions de protocoles
Sources :
(1) Masaru Tanaka et al. (2021). Co-Players in Chronic Pain: Neuro-inflammation and the Tryptophan-Kynurenine Metabolic Pathway. Biomedicines 2021, 9, 897.
(2) Fasano, A. (2012). Zonulin and its regulation of intestinal barrier function: The biological door to inflammation, autoimmunity, and cancer. Physiological Reviews, 91(1), 151–175.
(3) Gao, J., Xu, K., Liu, H., Liu, G., Bai, M., Peng, C., … & Li, T. (2018). Impact of the gut microbiota on intestinal immunity mediated by tryptophan metabolism. Frontiers in Cellular and Infection Microbiology, 8, 13.
(4) Calabrese, V., et al. (2021). Neuro-inflammation and neuropathic pain: from mechanisms to therapeutic targets. Journal of Neuro-inflammation, 18, 100.
(5) Ji, R.-R., Nackley, A., Huh, Y., Terrando, N., & Maixner, W. (2016). Neuro-inflammation and central sensitization in chronic and widespread pain. Anesthesiology, 126(3), 830–842.
(6) Banafshe, H. R., Ashtiani, H. R., & Mahmoudi, M. (2018). The role of liver detoxification in pain management. Journal of Pain Research, 11, 1397–1408.
(7) Zhang, Q., et al. (2019). Glutathione metabolism and its implications for pain and neuro-inflammation. Journal of Neurochemistry, 148(2), 167–181.
(8) McEwen, B. S. (2017). Neurobiological and systemic effects of chronic stress. Chronic Stress, 1, 2470547017692328.
(9) Liu, Y., Wang, L., Pan, X., Wang, C., & Wang, Z. (2020). Chronic stress impairs prefrontal cortex synaptic plasticity and cognitive function via NMDA receptor-dependent mechanisms. Neuroscience, 435, 135–145.
(10) Calabrese, F., Rossetti, A. C., Racagni, G., Gass, P., & Riva, M. A. (2021). Stress-induced neuro-inflammation: Mechanisms and new pharmacological targets. Neuroscience & Biobehavioral Reviews, 125, 437–455.
(11) Ji, R. R., Xu, Z. Z., & Gao, Y. J. (2016). Emerging targets in neuro-inflammation-driven chronic pain. Nature Reviews Drug Discovery, 13(7), 533–548.
(12) Schwartz, M., & Quintana, F. J. (2020). The kynurenine pathway in neurological disorders. Trends in Neurosciences, 43(12), 969–978.
(13) Schwartz, M., & Quintana, F. J. (2020). The role of the kynurenine pathway of tryptophan metabolism in inflammation: Mechanisms and therapeutic implications. Journal of Clinical Investigation, 130(5), 1985–1995.
(14) Sheng, J., Liu, S., Wang, Y., Cui, R., & Zhang, X. (2017). The link between depression and chronic pain: Neural mechanisms in the brain. Neural Plasticity, 2017, 9724371.
(15) Bäckryd, E., Tanum, L., Lind, A. L., Larsson, A., & Gordh, T. (2017). Evidence of both systemic inflammation and neuro-inflammation in fibromyalgia patients, as assessed by a multiplex protein panel applied to cerebrospinal fluid and plasma. Journal of Pain Research, 10, 515–525.
(16) Uçeyler, N., Häuser, W., & Sommer, C. (2011). Systematic review with meta‐analysis: cytokines in fibromyalgia syndrome. Rheumatology, 50(3), 534–543.
(17) Loggia, M. L., Berna, C., Kim, J., Cahalan, C. M., Gollub, R. L., Wasan, A. D., Harris, R. E., Edwards, R. R., & Napadow, V. (2015). Disrupted brain circuitry for pain-related reward/punishment in fibromyalgia. Brain, Behavior, and Immunity, 52, 149–158.
(18) Schäfers, M., Svensson, C. I., Sommer, C., & Sorkin, L. S. (2003). Tumor necrosis factor-alpha induces mechanical allodynia after spinal nerve ligation by activation of p38 MAPK in primary sensory neurons. Pain, 105(1–2), 205–213.
(19) Haroon, E., Fleischer, C. C., Felger, J. C., Chen, X., Woolwine, B. J., & Miller, A. H. (2016). Conceptual convergence: increased inflammation is associated with increased basal ganglia glutamate in patients with major depression. Molecular Psychiatry, 21(10), 1351–1357.
(20) Ridker, P. M., Hennekens, C. H., Buring, J. E., & Rifai, N. (2000). C-reactive protein and other markers of inflammation in the prediction of cardiovascular disease in women. The New England Journal of Medicine, 342(12), 836–843.
(21) Tóthová, C., Nagy, O., & Kovac, G. (2022). Serum protein electrophoresis and its diagnostic use in clinical practice: A review. Frontiers in Veterinary Science, 9, 853482.
(22) Calder, P. C. (2011). Fatty acids and inflammation: The cutting edge between food and pharma. Volume 668, Supplement 1, Pages S50-S58
(23) Ganz, T., & Nemeth, E. (2021). Iron homeostasis in host defence and inflammation. Nature Reviews Immunology, 21(1), 26–36.
(24) Ho, P. I., Ortiz, D., Rogers, E., & Shea, T. B. (2002). Multiple aspects of homocysteine neurotoxicity: glutamate excitotoxicity, kinase hyperactivation and DNA damage. Journal of Neuroscience Research, 70(5), 694–702.
(25) Fasano, A. (2020). Zonulin and its regulation of intestinal barrier function: the biological door to inflammation, autoimmunity, and cancer. Cellular and Molecular Gastroenterology and Hepatology, 10(1), 39–46.
(26) Ghosh, S. S., Wang, J., Yannie, P. J., & Ghosh, S. (2020). Intestinal barrier dysfunction, LPS translocation, and disease development. Journal of Endocrinology, 247(1), R13–R34.
(27) Schertzer, J. D., & Klip, A. (2021). Host immune activation by LPS through TLR4–A bridge to insulin resistance and metabolic disease. Cell Metabolism, 33(4), 659–660.
(28) Lang Illievich, K., Klivinyi, C., Lasser, C., Brenna, C. T. A., Szilagyi, I. S., & Bornemann Cimenti, H. (2023). Palmitoylethanolamide in the treatment of chronic pain: A systematic review and meta-analysis of double-blind randomized controlled trials. Nutrients, 15(6), 1350.
(29) Klipinyi, C., Lasser, C., & Bornemann Cimenti, H.-C. (2022). Central and peripheral effects of ultramicronized palmitoylethanolamide in healthy subjects. Nutrients, 14(19), 4084.
(30) Grzanna, R., Lindmark, L., & Frondoza, C. G. (2005). Ginger—An herbal medicinal product with broad anti-inflammatory actions. Journal of Medicinal Food, 8(2), 125–132.
(31) Tripathi, S., Bruch, D., & Kittur, D. S. (2008). Ginger extract inhibits LPS induced macrophage activation and function. BMC Complementary and Alternative Medicine, 8, 1.
(32) Infantino, M., & Di Giacomo, R. (2020). Clinical trials on pain-lowering effect of ginger: A narrative review. Acta Bio Medica: Atenei Parmensis, 91(11-S), e2020013.
(33) Dedov, V. N., Tran, V. H., Duke, C. C., & Ginger, S. (2002). Gingerols: A novel class of vanilloid receptor (VR1) agonists. British Journal of Pharmacology, 137(6), 793–798.
(34) Rahmani, A. H., Shabrmi, F. M. A., & Aly, S. M. (2014). Active ingredients of ginger as potential candidates in the prevention and treatment of diseases via modulation of biological activities. International Journal of Physiology, Pathophysiology and Pharmacology, 6(2), 125.
(35) Bridges, A. R., McCracken, L. M., & Droney, J. (2022). Omega-3 fatty acids and chronic pain: A review of the current evidence. Journal of Pain Research, 15, 1581–1594.
(36) Romay, C., Armesto, J., Remirez, D., González, R., Ledón, N., & García, I. (2003). Antioxidant and anti-inflammatory properties of C-phycocyanin from blue-green algae. Inflammopharmacology, 11(3), 255–265.
(37) Benedetti, S., Benvenuti, F., Scoglio, S., & Canestrari, F. (2020). Clinical evaluation of the anti-inflammatory and pain-relieving effects of a natural extract of spirulina: A pilot study on osteoarthritis. Clinical Nutrition ESPEN, 35, 159–165.
(38) Lopresti, A. L., & Drummond, P. D. (2014). Saffron (Crocus sativus) for depression: A systematic review of clinical studies and examination of underlying antidepressant mechanisms of action. Human Psychopharmacology: Clinical and Experimental, 29(6), 517–527.
(39) Shafiee, M., Arekhi, S., Omranzadeh, A., & Sahebkar, A. (2018). Saffron in the treatment of depression, anxiety and other mental disorders: Current evidence and potential mechanisms of action. Journal of Affective Disorders, 227, 330–337.
Document réservé à l’usage des praticiens de santé.
